题目内容
为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末.这种粉末是一种除氧剂.该粉末没有失效时呈黑色,失效后带有红棕色.为了确定该粉末的成分,小明做出了以下的猜想:
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格.
试验操作 试验现象 猜想是否成立
实验1 加入足量的硫酸铜溶液 猜想1:不成立
实验2 加入足量的 猜想2:成立
实验3 用磁铁吸引 粉末被全部吸引 猜想3:
交流与反思:
(1)根据失效后的颜色判断,该粉末失效的原因是 ,变质后得到的红棕色粉末的主要成分是 (填物质的化学式).
(2)采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示) .
考点: 猜想与事实验证;化学实验方案设计与评价;金属的化学性质;一氧化碳还原氧化铁;碳的化学性质;书写化学方程式、文字表达式、电离方程式.菁优网版权所有
专题: 实验性简答题;压轴实验题;填写实验报告题;物质的鉴别题.
分析: 根据猜想可知,黑色粉末可能为木炭粉、铁粉中的一种或两种的混合物,可利用铁粉与木炭粉性质的差别,对固体粉末的组成进行检验;
(1)由于铁粉在潮湿的空气中可与氧气、水发生反应而形成红综色的铁锈,因此失效后带有红棕色;
(2)氧化铁在高温条件下可与CO反应而生成铁和二氧化碳,因此,可把失效的粉末在高温下与CO反应而“再生”.
解答: 解:由于木炭不能与硫酸铜发生反应而铁粉可以置换出硫酸铜中的铜,因此,加入足量的硫酸铜溶液出现粉末变成红色现象时,即可说明猜想1不成立;
由于木炭不能与稀盐酸反应而铁粉可与稀盐酸反应形成硫酸亚铁溶液,同时放出氢气,因此,把黑色粉末放入足量稀盐酸时,出现黑色粉末溶解并放出气体时,可说明猜想2成立;
磁铁可以吸引铁粉而不能吸引木炭粉,用磁铁吸引时出现粉末全部被吸起,可说明猜想3不成立;
故答案为:
实验操作 实验现象 猜想是否成立
实验1 黑色粉末变成红色
实验2 稀盐酸 黑色粉末逐渐溶解,有大量的气泡产生
实验3 猜想3:不成立
(1)铁在潮湿的空气中生锈可形成红色的铁锈而失效;铁锈的主要成分为氧化铁,其化学式为;
故答案为:铁与空气中的氧气和水反应生成了铁锈;Fe2O3;
(2)使失效的粉末“再生”可在高温条件下,使用CO还原氧化铁而等到铁粉,达到“再生”的目的;
故答案为:3CO+Fe2O3 2Fe+3CO2.
2Fe+3CO2.
点评: 要对物质组成的猜想进行验证时,可根据所猜测的物质组成成分性质的不同,选择适当的试剂进行实验验证.

甲、乙、丙、丁表示四种物质,其微观示意图见下表,甲和乙在一定条件下反应生成丙丁。下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
|
| 微观示意图 |
|
|
|
|
A.甲、丁的化学式相同
B.只有丙物质属于单质
C.若16g乙参加反应,则生成的丙质量为32g
D.反应中,反应物分子中所含氧原子总数是生成物分子中所含氧原子总数的2倍



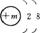 ,则下列各式正确的是( )
,则下列各式正确的是( )