题目内容
3.某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究【提出问题】二氧化碳是与氢氧化钠反应,还是微溶于水中?
【查阅资料】①15℃时,101KPa时,二氧化碳的溶解度如表;
| 溶剂 | 水 | 酒精 |
| 1 溶解度 | 1.0 | 0.3 |
③通常情况下,稀溶液的体积约等于溶剂的体积.
【实验设计】在15℃、101KPa时,制取二氧化碳并用于实验甲、实验乙.
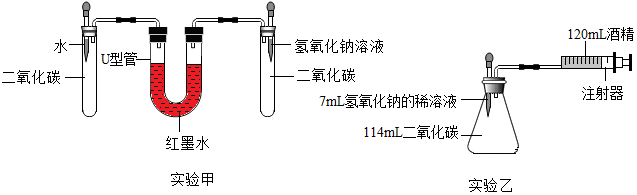
【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是CO2+2NaOH=Na2CO3+H2O,那么氢氧化钠应密封保存.
(2)实验前,两套装置都进行了气密性检查.实验乙装置气密性检查的方法是将注射器活塞往外拉出一段(或者往里推一段),一会儿后观察其是否回到远处.若回到远处,则气密性良好.
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是红墨水液面左边降低,右边升高,最终右边高于左边.
(4)实验乙中,将氢氧化钠溶液完全滴入锥形瓶中,注射器活塞会自动向内移动并将酒精推入锥形瓶中,还可能观察到的现象是生成白色浑浊或者沉淀.
(5)实验乙结束后,注射器中酒精体积为20mL,则锥形瓶和胶头滴管中剩余的二氧化碳体积为14mL,与氢氧化钠反应的二氧化碳体积为63mL.
分析 (1)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(2)由于注射器摩擦力很小,且装置本身就是密闭体系,所以推拉注射器活塞后装置气密性良好的情况下都能回到原位置;
(3)根据氢氧化钠会与二氧化碳反应,二氧化碳会与水反应,但是二氧化碳与氢氧化钠溶液反应后,压强的变化幅度大进行分析;
(4)根据氢氧化钠与二氧化碳反应后装置内的压强减少速度快,但是碳酸钠在酒精中是微溶的进行分析;
(5)根据二氧化碳在酒精中的溶解度是0.3,在水中的溶解度为1进行分析;
解答 解:首先要明确气体的溶解度是体积而不是质量,是单位体积的溶剂溶解的气体的体积.
(1)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O,所以氢氧化钠应密封保存;
(2)实验前,两套装置都进行了气密性检查.实验乙装置气密性检查的方法是 将注射器活塞往外拉出一段(或者往里推一段),一会儿后观察其是否回到远处.若回到远处,则气密性良好(其他合理也可)
(3)氢氧化钠会与二氧化碳反应,二氧化碳会与水反应,但是二氧化碳与氢氧化钠溶液反应后,压强的变化幅度大,所以实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是:右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,右侧液面仍高于左侧;
(4)氢氧化钠与二氧化碳反应后装置内的压强减少速度快,但是碳酸钠在酒精中是微溶的,所以将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,实验乙中,还可能观察到的现象是在锥形瓶中观察到白色浑浊或者沉淀;
(5)锥形瓶加上胶头滴管总体积为121mL,由于右侧进入的酒精的体积为100mL,而挤压后胶头滴管中的7mL氢氧化钠溶液也进入了锥形瓶,所以锥形瓶和胶头滴管内液体总计7mL+100mL=107mL,而锥形瓶加上胶头滴管总体积为121mL,所以剩余的二氧化碳的体积为121mL-107mL=14mL.溶液在氢氧化钠溶液中的水的二氧化碳的质量为7mL×1=7mL.溶解在酒精中的二氧化碳体积为100mL×0.3=30mL,所以和氢氧化钠反应的二氧化碳的体积为114mL-14mL(剩余的)-7mL(溶解于水的)-30mL(溶解于酒精的)=63mL.
故答案为:
(1)CO2+2NaOH=Na2CO3+H2O; 密封;
(2)将注射器活塞往外拉出一段(或者往里推一段),一会儿后观察其是否回到远处.若回到远处,则气密性良好(其他合理即可).
(3)红墨水液面左边降低,右边升高,最终右边高于左边.
(4)生成白色浑浊或者沉淀.
(5)14;63.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答,本题难度较大.

 中考解读考点精练系列答案
中考解读考点精练系列答案金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是 。

A.铝原子的质子数为13 |
B.在化合物中铝通常显+3价 |
C.铝是地壳中含量最多的元素 |
D.铝可作导线是由于它具有良好的导电性 |
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和实验探究。

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2② Zn (NO3)2、AgNO3③ Zn (NO3)2、Cu(NO3)2④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是 (填标号),其理由是 。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现 象 | 有关反应的化学方程式 |
取少量固体B, | 有气泡产生 | |
鉴别下列物品方法不正确的是( )
选项 | 鉴别的物质 | 鉴别的方法 |
A | 冰和干冰 | 室温(20℃)放置,过一段观察是否有水渍 |
B | 水和双氧水 | 加二氧化锰,观察是否有气泡 |
C | 二氧化锰和氧化铜 | 观察颜色 |
D | 纯羊毛和化纤面料 | 灼烧闻气味 |
A. A B. B C. C D. D
| A. | 加速溶解 | B. | 引流 | C. | 防液飞溅 | D. | 转移固体 |
 将一定量的Zn粉加入一定量的AgNO3和Fe(NO3)2的混合溶液,得到的固体质量随时间的变化关系如图所示,下列说法不正确的是( )
将一定量的Zn粉加入一定量的AgNO3和Fe(NO3)2的混合溶液,得到的固体质量随时间的变化关系如图所示,下列说法不正确的是( )| A. | 当反应进行到t时,所得金属固体中的物质至少有两种 | |
| B. | 当反应进行到t时,取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 当反应进行到t时,此时取滤渣滴加稀盐酸,一定有气泡产生 | |
| D. | 当反应进行到t时,取反应后的滤液观察,滤液呈浅绿色 |
| A. | Al(OH)3 | B. | NH4Cl | C. | K3PO4 | D. | Fe2(SO4)3 |
| A. | 滤渣的质量一定大于a g | |
| B. | 若滤渣中含有单质Zn,则滤液一定是无色溶液 | |
| C. | 若向滤渣中加入足量的稀盐酸有气泡冒出,则滤渣中一定含有Ag、Cu、Fe | |
| D. | 若向滤液中加入足量的稀盐酸有白色沉淀产生,则滤液中的一定含有四种金属阳离子 |