题目内容
11.下列哪项含有化合价为-3价的原子团?( )| A. | Al(OH)3 | B. | NH4Cl | C. | K3PO4 | D. | Fe2(SO4)3 |
分析 根据化合物中正负化合价代数和等于零的原则计算出各原子团的化合价,然后进行比较即可.
解答 解:A、Al(OH)3中铝元素显-3价,氢氧根的化合价为-1价;故错误;
B、NH4Cl中氯元素显-1价,铵根的化合价为+1价;故错误;
C、K3PO4中钾元素显+1价,磷酸根的化合价为-3价;故正确;
D、Fe2(SO4)3铁元素显+3价,硫酸根的化合价为-2价;故错误.
故选C.
点评 解题时可以把原子团看成一种元素,从这个角度理解,可使计算简单化.

练习册系列答案
相关题目
3.某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究
【提出问题】二氧化碳是与氢氧化钠反应,还是微溶于水中?
【查阅资料】①15℃时,101KPa时,二氧化碳的溶解度如表;
②15℃时,在酒精中,氢氧化钠易溶,碳酸钠微溶.
③通常情况下,稀溶液的体积约等于溶剂的体积.
【实验设计】在15℃、101KPa时,制取二氧化碳并用于实验甲、实验乙.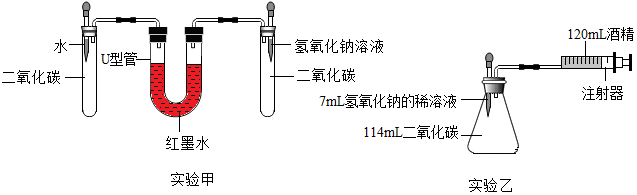
【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是CO2+2NaOH=Na2CO3+H2O,那么氢氧化钠应密封保存.
(2)实验前,两套装置都进行了气密性检查.实验乙装置气密性检查的方法是将注射器活塞往外拉出一段(或者往里推一段),一会儿后观察其是否回到远处.若回到远处,则气密性良好.
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是红墨水液面左边降低,右边升高,最终右边高于左边.
(4)实验乙中,将氢氧化钠溶液完全滴入锥形瓶中,注射器活塞会自动向内移动并将酒精推入锥形瓶中,还可能观察到的现象是生成白色浑浊或者沉淀.
(5)实验乙结束后,注射器中酒精体积为20mL,则锥形瓶和胶头滴管中剩余的二氧化碳体积为14mL,与氢氧化钠反应的二氧化碳体积为63mL.
【提出问题】二氧化碳是与氢氧化钠反应,还是微溶于水中?
【查阅资料】①15℃时,101KPa时,二氧化碳的溶解度如表;
| 溶剂 | 水 | 酒精 |
| 1 溶解度 | 1.0 | 0.3 |
③通常情况下,稀溶液的体积约等于溶剂的体积.
【实验设计】在15℃、101KPa时,制取二氧化碳并用于实验甲、实验乙.

【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是CO2+2NaOH=Na2CO3+H2O,那么氢氧化钠应密封保存.
(2)实验前,两套装置都进行了气密性检查.实验乙装置气密性检查的方法是将注射器活塞往外拉出一段(或者往里推一段),一会儿后观察其是否回到远处.若回到远处,则气密性良好.
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是红墨水液面左边降低,右边升高,最终右边高于左边.
(4)实验乙中,将氢氧化钠溶液完全滴入锥形瓶中,注射器活塞会自动向内移动并将酒精推入锥形瓶中,还可能观察到的现象是生成白色浑浊或者沉淀.
(5)实验乙结束后,注射器中酒精体积为20mL,则锥形瓶和胶头滴管中剩余的二氧化碳体积为14mL,与氢氧化钠反应的二氧化碳体积为63mL.
19.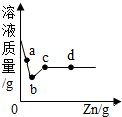 向一定质量AgNO3、Cu(NO3)2、KNO3的混合溶液中加入过量的Zn,溶液质量与加入Zn的质量关系如图所示.下列说法正确的是( )
向一定质量AgNO3、Cu(NO3)2、KNO3的混合溶液中加入过量的Zn,溶液质量与加入Zn的质量关系如图所示.下列说法正确的是( )
 向一定质量AgNO3、Cu(NO3)2、KNO3的混合溶液中加入过量的Zn,溶液质量与加入Zn的质量关系如图所示.下列说法正确的是( )
向一定质量AgNO3、Cu(NO3)2、KNO3的混合溶液中加入过量的Zn,溶液质量与加入Zn的质量关系如图所示.下列说法正确的是( )| A. | 取a点溶液,滴加稀盐酸,无白色沉淀 | |
| B. | c点溶液中溶质为Zn(NO3)2 | |
| C. | 若取c~d段固体,滴加稀盐酸,无气泡产生 | |
| D. | 取d点的固体有3种 |
6.地壳中含量最多的金属元素符号是( )
| A. | Si | B. | Fe | C. | Al | D. | Ca |
16.氮的化合价为+5的氧化物是( )
| A. | KNO3 | B. | NO2 | C. | N2O5 | D. | NH3 |
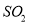 的严重污染,环保部门立即派出了飞机喷洒X粉末,快速降低空气中的
的严重污染,环保部门立即派出了飞机喷洒X粉末,快速降低空气中的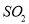 含量,该过程发生的化学反应是
含量,该过程发生的化学反应是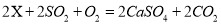 ,则X的化学式是( )
,则X的化学式是( )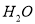 B.
B. 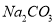 C.
C. 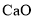 D.
D. 
 金属及其制品是现代生活中常见的材料,请回答下列问题
金属及其制品是现代生活中常见的材料,请回答下列问题