题目内容
18.有一包固体,可能由硝酸铜、硫酸钠、碳酸氢钠、氢氧化钠、氯化钠中的一种或几种组成.为了探究该固体的组成,某化学小组设计并开展了以下实验: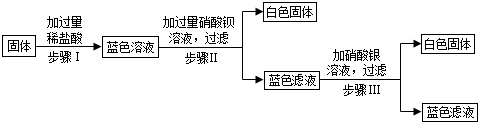
已知,步骤Ⅰ中固体全部消失,溶液呈蓝色,无气泡产生;步骤Ⅱ、Ⅲ均可观察到有白色沉淀生成.
请回答下列问题:
(1)原固体中一定不含有的物质是碳酸氢钠(写化学式,下同),证据为向固体中加过量稀盐酸,无气泡产生.
(2)小组中甲同学认为通过该实验可以确定氯化钠的存在,乙同学不同意甲同学的观点,他的理由是由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠,这时丙同学说可以将实验稍作改动即可判断氯化钠是否存在,他的做法是将步骤Ⅰ中的稀盐酸改成稀硝酸.
(3)步骤 III所得蓝色滤液中一定含有的溶质有硝酸、硝酸钠、硝酸钡、硝酸铜.
分析 根据固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;又因为无气泡产生,所以固体中一定不含有碳酸氢钠;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;步骤Ⅲ中加入硝酸银溶液,出现白色沉淀,则该白色沉淀为氯化银,由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠进行分析.
解答 解:固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜;又因为无气泡产生,所以固体中一定不含有碳酸氢钠;步骤Ⅱ加入过量硝酸钡产生白色沉淀,说明固体中一定含有硫酸钠;步骤Ⅲ中加入硝酸银溶液,出现白色沉淀,则该白色沉淀为氯化银,由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠,所以
(1)固体加过量稀盐酸无气泡产生,所以固体中一定不含有碳酸氢钠;
(2)小组中甲同学认为通过该实验可以确定氯化钠的存在,乙同学不同意甲同学的观点,理由是:由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠,这时丙同学说可以将实验稍作改动即可判断氯化钠是否存在,他的做法是:将步骤Ⅰ中的稀盐酸改成稀硝酸;
(3)根据向固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜,所以蓝色滤液中一定含有硝酸铜和盐酸;加入过量硝酸钡,说明硝酸钡有剩余,所以蓝色滤液中一定含有硝酸钡;硝酸钡和硫酸钠反应生成硝酸钠和硫酸钡沉淀,所以蓝色滤液中一定含有硝酸钠,盐酸和硝酸银反应生成氯化银沉淀和硝酸.
故答案为:(1)碳酸氢钠,向固体中加过量稀盐酸,无气泡产生;
(2)由于一开始加入过量稀盐酸,所以溶液中一定有氯离子,所以会生成氯化银沉淀,但不能确定一定含有氯化钠,将步骤Ⅰ中的稀盐酸改成稀硝酸;
(3)硝酸、硝酸钠、硝酸钡、硝酸铜.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

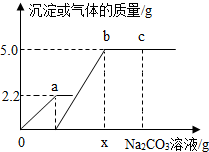 向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液.反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法不正确的是( )| A. | 图中oa段表示生成气体的过程 | B. | b点溶液中溶质有2种 | ||
| C. | c点溶液的pH>7 | D. | x值为106.0 |
| A. | 积极植树造林 | B. | 禁止使用化石燃料 | ||
| C. | 随意丢弃废旧电池 | D. | 大量使用聚乙烯塑料 |
| A. | 光合作用 | B. | 浓硫酸做干燥剂 | ||
| C. | 用食醋除水垢 | D. | 用灼烧法鉴别羊毛和合成纤维 |
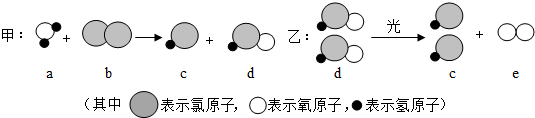
下列说法正确的是( )
| A. | 物质a、b、c 分别是氧化物、单质和酸 | |
| B. | 气体b 能用排水法收集 | |
| C. | 甲、乙两反应中各有一种元素的化合价发生改变 | |
| D. | 气体e 具有可燃性 |