题目内容
3. 硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )
硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )| A. | 硝酸钾的溶解度一定大于氯化钾的溶解度 | |
| B. | t℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等 | |
| C. | 降低温度可使接近饱和的硝酸钾溶液变饱和 | |
| D. | 60℃时,100 g水中加入90 g硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液 |
分析 A、根据物质溶解度的比较方法考虑;
B、根据饱和溶液质量分数的计算考虑;
C、根据硝酸钾的溶解度与温度的关系考虑;
D、根据60℃时,硝酸钾的溶解度考虑溶质是否全部溶解
解答 解:A、物质溶解度的比较必须有温度的限制,否则不能比较,故A错;
B、饱和溶液的质量分数的计算公式:$\frac{溶解度}{100g+溶解度}$×100%,t℃时,硝酸钾和氯化钾溶解度相等,两种饱和溶液的溶质质量分数一定相等,但本题没说是否饱和,故B错;
C、由于硝酸钾的溶解度随着温度的降低而减小,所以降温能由不饱和变为饱和溶液,故C正确;
D、由图示可知60℃时,硝酸钾的溶解度大于90g,所以60℃时100 g水中加入90 g硝酸钾,充分搅拌,可得到硝酸钾的不饱和溶液,故D错.
故选C.
点评 本题容易出错的地方是看到t℃时,硝酸钾和氯化钾的溶解度相等,就误认为溶质质量分数相等,应该对于饱和溶液才行.

练习册系列答案
相关题目
14.“酸雨”大家一定听说过,可“碱雨”呢?1958年以来,有人陆续在美国等地收集到碱性雨水(即“碱雨”).“碱雨”是如何形成的?原来,人们向植物施铵态氮肥时,由于某些干旱地区土壤多呈碱性,使得铵态氮肥转化为氨气进入大气,进入大气中的氨遇雨而降便形成了“碱雨”.回答下列问题:
(1)“碱雨”的pH大于7(填“大于”“小于”或“等于”).
(2)“酸雨”是因为工业生产过程中向大气中大量排放二氧化硫、氮氧化物造成的.
(3)NH4HCO3受热易分解为氨气、水和二氧化碳,其反应的化学方程式为NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(4)请为施用铵态氮肥提出一条合理措施.不能向碱性土壤中施加.
【探究创新】
小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:
【提出问题】温度较高时,碳酸氢铵能分解吗?产物是什么?
【猜想假设】碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气.
【实验设计】小明设计了如图所示的装置进行实验(夹持装置省略).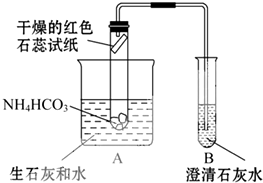
(1)根据现象干燥的红色石蕊试纸变蓝,证明实验后生成了水和氨气.
(2)装置B中澄清石灰水变浑浊,证明产物中有二氧化碳.
(3)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成.请你帮她设计并完成验证B中产物的实验:
【实验结论】碳酸氢铵受热易分解,其反应的化学方程式为NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
【实验评价】在上述同学们探究活动中,你最欣赏的是小明同学用生石灰和水反应放出的热量做热源.
【实验反思】根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是防潮、避光、避热、密封等.
(1)“碱雨”的pH大于7(填“大于”“小于”或“等于”).
(2)“酸雨”是因为工业生产过程中向大气中大量排放二氧化硫、氮氧化物造成的.
(3)NH4HCO3受热易分解为氨气、水和二氧化碳,其反应的化学方程式为NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(4)请为施用铵态氮肥提出一条合理措施.不能向碱性土壤中施加.
【探究创新】
小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:
【提出问题】温度较高时,碳酸氢铵能分解吗?产物是什么?
【猜想假设】碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气.
【实验设计】小明设计了如图所示的装置进行实验(夹持装置省略).

(1)根据现象干燥的红色石蕊试纸变蓝,证明实验后生成了水和氨气.
(2)装置B中澄清石灰水变浑浊,证明产物中有二氧化碳.
(3)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成.请你帮她设计并完成验证B中产物的实验:
| 实验步骤 | 实验现象 | 反应的化学方程式 |
【实验评价】在上述同学们探究活动中,你最欣赏的是小明同学用生石灰和水反应放出的热量做热源.
【实验反思】根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是防潮、避光、避热、密封等.
11.锌粉、铝粉、铁粉、镁粉的混合物3.2 g与一定质量的溶质质量分数为25%的稀硫酸恰好完全反应,将反应后的混合物蒸干水分得固体11 g,则反应中生成氢气的质量为( )
| A. | 0.15 g | B. | 0.20 g | C. | 0.30 g | D. | 0.45 g |
15.新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图所示.
请根据相关信息计算回答:
(1)帕拉米韦由碳、氢、氮、氧四种元素组成,其中氢、氮的原子个数比为7:1;
(2)帕拉米韦的化学式为C15H28O□N4,□内氧原子的个数是4;
(3)帕拉米韦中氧元素的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
(4)成人禽流感患者,每天应注射帕拉米韦注射液6支.
请根据相关信息计算回答:
| 药品名:帕拉米韦注射液 化学式:C15H28O□N4 相对分子质量:328 适应症:H7N9禽流感 成人用量:75mg/次2次/日 帕拉米韦含量:25mg/支 |
(2)帕拉米韦的化学式为C15H28O□N4,□内氧原子的个数是4;
(3)帕拉米韦中氧元素的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
(4)成人禽流感患者,每天应注射帕拉米韦注射液6支.
17.下列实验操作中正确的是( )
| A. |  闻气体味道 | B. |  稀释浓硫酸 | C. |  取用木炭粉末 | D. |  过滤 |
 实验室用如图所示装置制取蒸馏水.请据此回答有关问题:
实验室用如图所示装置制取蒸馏水.请据此回答有关问题: 下列是探究空气中氧气所占体积的实验
下列是探究空气中氧气所占体积的实验