题目内容
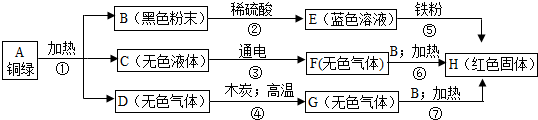
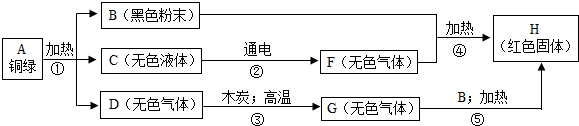
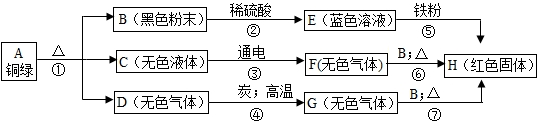
某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤探究铜绿的组成.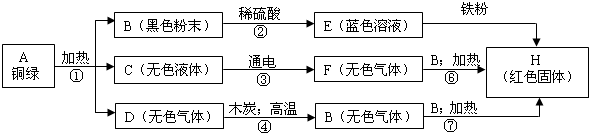
(1)推断B、C是何种物质,写出它们的化学式:B
(2)从图中转化关系可以初步判断,铜绿的组成元素有
(3)图中第③步反应的化学方程式是
(4)图中第⑤步反应的化学方程式是
分析:根据物质的相互反应规律和特殊的现象找出突破点:E为蓝色溶液,E中一定含有有铜离子,B为黑色粉末,和稀硫酸反应生成E,可知B为氧化铜,E为硫酸铜,E和铁反应生成红色固体H,H为铜,C 在通电条件下可分解,则C为水,水通电生成的气体F和氧化铜加热生成铜,说明F具有还原性,则F为氢气.G和氧化铜加热生成铜,说明G具有还原性,具有还原性的气体主要是氢气和一氧化碳,G是由无色气体D和木炭高温反应生成的,G中含有碳元素,则G为一氧化碳,D为二氧化碳.
解答:解:(1)黑色粉末B和稀硫酸反应生成蓝色溶液E,E中一定含有铜离子,则黑色粉末B为氧化铜,蓝色溶液E为硫酸铜溶液,硫酸铜和铁反应生成红色固体H,则H为铜,无色液体C在通电条件下能分解,则C为水,G和氧化铜加热能生成铜,说明G具有还原性,具有还原性的气体一般是氢气和一氧化碳,G是由D和木炭高温反应生成的,G中含有碳元素,G为一氧化碳,则D为二氧化碳;
(2)因为B是氧化铜,C是水,D是二氧化碳,根据化学反应前后元素的种类不变可知铜绿的组成元素为 Cu O C H
(2)无色液体C在通电条件下能发生反应,可知无色液体C为水,化学方程式为:2H2O
2H2↑+O2↑
(3)蓝色硫酸铜溶液和铁反应的化学方程式为:Fe+CuSO4=FeSO4+Cu
故答案为:(1)CuO;H2O;
(2)Cu、H、O、C
(3)2H2O
2H2↑+O2↑
(4)Fe+CuSO4=FeSO4+Cu
(2)因为B是氧化铜,C是水,D是二氧化碳,根据化学反应前后元素的种类不变可知铜绿的组成元素为 Cu O C H
(2)无色液体C在通电条件下能发生反应,可知无色液体C为水,化学方程式为:2H2O
| ||
(3)蓝色硫酸铜溶液和铁反应的化学方程式为:Fe+CuSO4=FeSO4+Cu
故答案为:(1)CuO;H2O;
(2)Cu、H、O、C
(3)2H2O
| ||
(4)Fe+CuSO4=FeSO4+Cu
点评:解答本类型题的关键是根据明显现象找到突破点,然后根据突破点逐步确定每种物质.找突破点要根据物质的特殊性质或典型的反应规律.

练习册系列答案
相关题目