题目内容
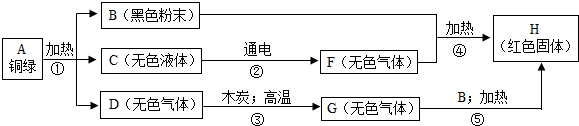
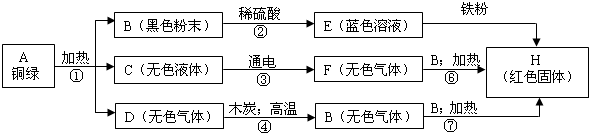
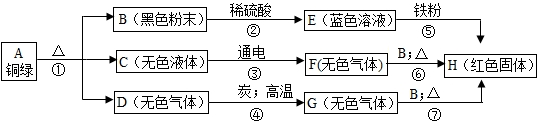
某兴趣小组从铜器上取下绿色粉未,设计如下实验步骤进行探究铜绿的组成.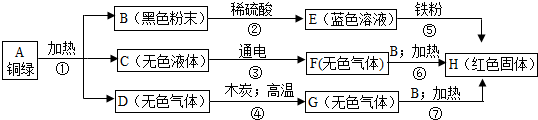
(1)写出:B物质的化学式
(2)我国古代有“曾青得铁则化为铜”的记载,这是现代湿法冶金的原理.这与上述实验方案中第
(3)写出第③步反应的化学方程式是
(4)在设计方案中有三种冶炼铜的方法,通过比较请从资源、能源或环境等方面,说出其中一种方案所具有的优点:
分析:E为蓝色溶液,E中一定含有有铜离子,B为黑色粉末,和稀硫酸反应生成E,可知B为氧化铜,E为硫酸铜,E和铁反应生成红色固体H,H为铜,C 在通电条件下可分解,则C为水,水通电生成的气体F和氧化铜加热生成铜,说明F具有还原性,则F为氢气.G和氧化铜加热生成铜,说明G具有还原性,具有还原性的气体主要是氢气和一氧化碳,G是由无色气体D和木炭高温反应生成的,G中含有碳元素,则G为一氧化碳,D为二氧化碳.
解答:解:(1)黑色粉末B和稀硫酸反应生成蓝色溶液E,E中一定含有铜离子,则黑色粉末B为氧化铜,蓝色溶液E为硫酸铜溶液,硫酸铜和铁反应生成红色固体H,则H为铜,无色液体C在通电条件下能分解,则C为水,G和氧化铜加热能生成铜,说明G具有还原性,具有还原性的气体一般是氢气和一氧化碳,G是由D和木炭高温反应生成的,G中含有碳元素,G为一氧化碳,则D为二氧化碳,根据化学反应前后元素的种类不变可知铜绿的组成元素为 Cu O C H
故选CuO Cu、O、C、H
(2)湿发冶金术的原理是Fe+CuSo4=FeSO4+Cu,故答案为:⑤Fe+CuSo4=FeSO4+Cu
(3)无色液体C在通电条件下能发生反应,可知无色液体C为水,故答案为:2H2O
2H2↑+O2↑
(4)一般不加热,操作简便,污染少,节约能源的方案为好的方案,故答案为:用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热.
故选CuO Cu、O、C、H
(2)湿发冶金术的原理是Fe+CuSo4=FeSO4+Cu,故答案为:⑤Fe+CuSo4=FeSO4+Cu
(3)无色液体C在通电条件下能发生反应,可知无色液体C为水,故答案为:2H2O
| ||
(4)一般不加热,操作简便,污染少,节约能源的方案为好的方案,故答案为:用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热.
点评:解本类型题的关键是根据明显现象找到突破点,然后根据突破点逐步确定每种物质.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目