题目内容
12g碳和32g氧气恰好完全反应,可生成二氧化碳 g,若生成11g二氧化碳,则需要 g碳在 g氧气中恰好完全燃烧.
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应遵循质量守恒定律,即参加反应的物质质量总和等于反应后生成的物质质量总和.
解答:解:12g碳和32g氧气恰好完全反应,根据质量守恒定律可知,生成二氧化碳的质量为:12g+32g=44g;
若生成11g二氧化碳,则需要的碳的质量为:12g÷4=3g;
需要氧气的质量为:32g÷4=8g.
故填:44;3;8.
若生成11g二氧化碳,则需要的碳的质量为:12g÷4=3g;
需要氧气的质量为:32g÷4=8g.
故填:44;3;8.
点评:化学反应遵循质量守恒定律,当生成物的质量成倍的增加或减小时,反应物的质量也成倍的增加或减小.

练习册系列答案
相关题目
下列关于碳单质的说法正确的是( )
| A、C60的相对分子质量是720 |
| B、石墨很软,不能用于制造石墨电极 |
| C、石墨、金刚石和C60都是由碳元素组成,结构相同 |
| D、木炭具有还原性,常温下可以将氧化铜中的铜还原出来 |
酸雨是酸性降雨,其pH应该是( )
| A、<5.6 | B、=14 |
| C、=7 | D、>9.6 |
2.8g某物质R与9.6g氧气恰好完全反应,化学方程式为:R+3O2
2XO2+2H2O,下列判断正确的是( )
| ||
| A、R的相对分子质量为28g |
| B、R中一定含X元素、氢元素,可能含有氧元素 |
| C、XO2中X元素与氧元素的质量比为1:2 |
| D、生成的XO2和H2O的质量比为22:9 |
下列图示实验操作中,正确的是( )
A、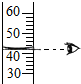 读取液体体积 |
B、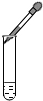 向试管中添加液体 |
C、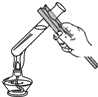 给液体加热 |
D、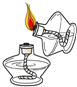 点燃酒精灯 |
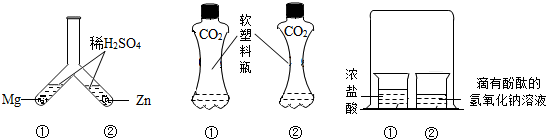
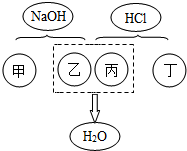
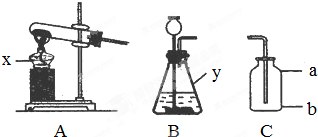
 某同学为研究动物的呼吸作用,用如图装置进行实验.实验过程中将观察到:澄清石灰水
某同学为研究动物的呼吸作用,用如图装置进行实验.实验过程中将观察到:澄清石灰水