题目内容
5.某同学在四个烧杯中分别做氯化铵的溶解实验,请依据表格中的数据回答:| 烧杯序号 | 温度/℃ | 水的质量/g | 氯化铵质量/g | 溶液质量/g |
| ① | 20 | 100 | 20 | a |
| ② | 20 | 100 | 40 | 137.2 |
| ③ | 40 | 100 | 40 | 140 |
| ④ | 60 | 100 | 50 | 150 |
(2)将烧杯①所得溶液稀释成溶质质量分数为10%的溶液,需要加水80g;
(3)上述烧杯中的溶液不能确定是否达到饱和状态的是③④(填序号);
(4)若将烧杯②中溶液升温到40℃(不考虑水的蒸发),下列各量一定变大的是ACD.
A.溶质质量 B.溶剂质量 C.溶解度 D.溶质的质量分数.
分析 (1)由题意可知20℃时100g水最多溶解37.2g氯化铵进行解答;
(2)根据溶液稀释过程中溶质不变进行解答;
(3)根据饱和溶液的含义进行解答;
(4)根据烧杯②溶液是饱和溶液,有剩余溶质,升温后溶液质量增加进行解答.
解答 解:(1)由题意可知:烧杯②中20℃时100g水加入40g溶质,得到137.2g溶液,可知最多溶解37.2g氯化铵,所以20℃时,氯化铵的溶解度是37.2g;
(2)20℃时的溶解度是37.2g,则20g氯化铵在100g水中完全溶解,所以溶液的质量=20g+100g=120g,稀释过程中溶质的质量不变,设加水的质量为x,则有(120g+x)×10%=20g,解得x=80g;
(3)40℃时40g氯化铵在100g水中完全溶解,50℃时50g氯化铵在100g水中也完全溶解,所以不能判断是否为饱和溶液;
(4)若将烧杯②中溶液升温到40℃(不考虑水的蒸发),未溶解的氯化铵会继续溶解,则溶液中溶质质量增加、溶解度变大,溶剂质量不变,所以溶质的质量分数会增大,故选ACD;
故答案为:(1)37.2g;(2)80;(3)③④;(4)ACD.
点评 本题难度不是很大,主要考查了饱和溶液的判断、物质的溶解度及溶液的稀释问题,可培养学生分析问题、解决问题的能力.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
16.某同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究,请你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙;
猜想二:可能是CaCl2和Ca(OH)2;
猜想三:含有HCl和CaCl2.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
【方案评价】该同学与同学们通过讨论认为:
(1)方案一能证明猜想二正确,但不能证明猜想一正确.
(2)方案二可行.但该同学在记录时未记录完整,请你帮他将方案二补充完整.
【方案反思】方案一不能证明猜想一正确的理由是酚酞不变色还可能是含有盐酸和氯化钙.
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤即得只含有氯化钙的废液.
【结论】在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙;
猜想二:可能是CaCl2和Ca(OH)2;
猜想三:含有HCl和CaCl2.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中, 滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中, 逐滴加入碳酸钠溶液至过量 | 先有气泡冒出,然后会有沉淀 | 猜想三正确 |
(1)方案一能证明猜想二正确,但不能证明猜想一正确.
(2)方案二可行.但该同学在记录时未记录完整,请你帮他将方案二补充完整.
【方案反思】方案一不能证明猜想一正确的理由是酚酞不变色还可能是含有盐酸和氯化钙.
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤即得只含有氯化钙的废液.
【结论】在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量.
13.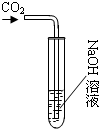 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
探究一:二氧化碳是否与氢氧化钠发生了化学反应?同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出
证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】贝贝为了验证自己的猜想,进行了如表实验,请你补充完整.
【实验反思】同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否反生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴边测定混合溶液的pH.请你分析上述方案中,为什么要“当测定pH小于或等于7,”才可证明发生反应了,其原因是排除因硫酸的加入,稀释氢氧化钠溶液而引起pH减小因素的干扰.
 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.探究一:二氧化碳是否与氢氧化钠发生了化学反应?同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出
证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】贝贝为了验证自己的猜想,进行了如表实验,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管中,加入足量CaCl2溶液,过滤 ②向滤液滴加适量酚酞 | ①产生白色沉淀 ②溶液变红 | 贝贝的猜想成立 |
20.除去下列物质中少量杂质(括号内为杂质),所用除去杂质的方法正确的是( )
| 选项 | 待提纯的物质 | 除去杂质的方法 |
| A. | FeSO4溶液(CuSO4) | 加入适量Zn粉,过滤 |
| B. | KCl( MnO2) | 加水溶解、过滤、洗涤、干燥 |
| C. | NaCl溶液(FeCl3) | 加入过量NaOH溶液,过滤 |
| D. | CO2(CO) | 通过灼热的足量的CuO |
| A. | A | B. | B | C. | C | D. | D |
13.下列能源属于可再生能源的是( )
| A. | 氢气 | B. | 煤 | C. | 石油 | D. | 天然气 |
 在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.
在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.