题目内容
8.调味剂的主要作用是补充、增强或增加食品的味道.食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH),与我们的生活密切相连.根据所学知识回答:(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和H+(填离子符号).
(2)食醋的酸味能促进人胃酸的分泌,胃酸的成分是HCl(填化学式).
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与CaCO3(填化学式)反应.
(4)若NaOH溶液溅到皮肤上,应用水冲洗后,再用食醋清洗.清洗过程中发生反应的化学方程式为CH3COOH+NaOH═CH3COONa+H2O.
(5)生活中常用酒来制取食醋,原理是酒中的CH3CH2OH在酶的作用下与空气中O2反应得到醋酸和另一种液体.已知在用酒制取食醋过程中,质量增加了16kg,则所得食醋中醋酸的质量为30kg.
分析 (1)根据醋酸的化学式可以判断醋酸在水溶液中解离出的离子;
(2)胃酸的主要成分为盐酸,可以据此解得该题;
(3)酸可以和碳酸盐发生反应,可以据此解答该题;
(4)氢氧化钠为碱,醋酸为酸,它们之间可以发生酸碱中和反应,可以据此解答;
(5)根据题给信息可以知道增加的质量为氧气的质量,可以据此结合反应的化学方程式求算出所得食醋的质量.
解答 解:(1)酸在水中可以电离醋酸根离子和氢离子,所以醋酸水溶液中能解离出CH3COO-和H+;
(2)胃酸的主要成分为盐酸,其化学式为HCl;
(3)酸可以和碳酸盐发生反应,鸡蛋壳和鱼骨中含有碳酸钙,其化学式为:CaCO3;
(4)氢氧化钠为碱,醋酸为酸,它们之间可以发生酸碱中和反应,该反应的化学方程式为:CH3COOH+NaOH═CH3COONa+H2O;
(5)设所得食醋中醋酸的质量为x
C2H5OH+O2═CH3COOH+H2O
32 60
16kg x
$\frac{32}{60}=\frac{16kg}{x}$
解得:x=30kg
故答案为:(1)H+;
(2)HCl;
(3)CaCO3;
(4)CH3COOH+NaOH═CH3COONa+H2O;
(5)30.
点评 要想解答好这类题目,首先,要理解和熟记醋酸的性质及醋酸的含量测定,以及与之相关的知识.然后根据所给的实验、问题情景,结合所学的相关知识和技能,细致地分析题意等,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.碳酸氢钠和碳酸氢铵是制作油条和油饼时常用的膨松剂,化学兴趣小组对这两种膨松剂受热后的产物进行了探究:
【查阅资料】1、碱石灰是氢氧化钠固体和氧化钙的混合物,不与氨气反应.
2、碳酸氢钠溶液能与氢氧化钙或氢氧化钡溶液反应,有沉淀产生.
3、碳酸氢盐易溶于水
【进行实验】按如图所示连接好装置(夹持仪器略去).
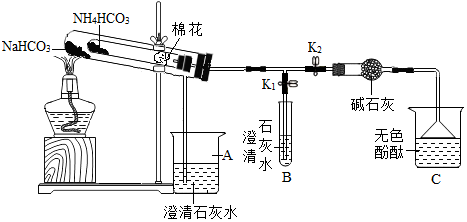
【实验反思】
(1)根据实验结果,化学兴趣小组的同学认为:与碳酸氢铵相比,碳酸氢钠更适宜作食品蓬松剂,其理由是碳酸氢铵受热分解会产生氨气,有刺激性的气味,且会污染空气.
(2)为了确定外层大试管内残留的该固体中有Na2CO3,接下来应进行实验是取少量残留固体于试管中,加入BaCl2溶液(合理即可),产生白色沉淀..
【查阅资料】1、碱石灰是氢氧化钠固体和氧化钙的混合物,不与氨气反应.
2、碳酸氢钠溶液能与氢氧化钙或氢氧化钡溶液反应,有沉淀产生.
3、碳酸氢盐易溶于水
【进行实验】按如图所示连接好装置(夹持仪器略去).

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 连接好装置,关闭K1,打开K2,微热左侧双层试管; | AC中出现气泡 | 装置的气密性良好. |
| 打开K1,关闭K2,停止加热. | A、B烧杯中的导管内均形成一段稳定的液柱. | ||
| ② | 在试管中加入两种膨松剂,打开K1,关闭K2,点燃酒精灯加热双层试管; | 内层小试管中白色固体明显减少,A、B中澄清的石灰水变浑浊. | 均有二氧化碳生成. |
| ③ | 关闭K1,打开K2; | 无色酚酞试液变红. | 碳酸氢铵分解有氨气产生. |
| ④ | 继续加热一段时间. | 内层小试管中固体消失,外层大试管中仍有固体残留. | 碳酸氢钠和碳酸氢铵的化学性质均是受热易分解. |
(1)根据实验结果,化学兴趣小组的同学认为:与碳酸氢铵相比,碳酸氢钠更适宜作食品蓬松剂,其理由是碳酸氢铵受热分解会产生氨气,有刺激性的气味,且会污染空气.
(2)为了确定外层大试管内残留的该固体中有Na2CO3,接下来应进行实验是取少量残留固体于试管中,加入BaCl2溶液(合理即可),产生白色沉淀..
16.某化学兴趣小组学习酸碱中和反应后,对稀盐酸与氢氧化钠溶液混合后的有关问题进行了如下探究.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
丁同学猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请将下列实验报告填写完整:
【反思交流】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)根据所学化学知识,要验证氢氧化钠溶液与稀盐酸混合后所得溶液中溶质的成分含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?a、c(填序号)
a.pH试纸 b.铜 c.锌粒 d.硝酸银溶液.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
丁同学猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中, 加入紫色石蕊溶液 | 溶液变红色 | 丙同学的猜想正确 |
| 取反应后的溶液于试管中, 加入硫酸铜溶液 | 有蓝色沉淀生成 | 丁同学的猜想正确 |
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)根据所学化学知识,要验证氢氧化钠溶液与稀盐酸混合后所得溶液中溶质的成分含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?a、c(填序号)
a.pH试纸 b.铜 c.锌粒 d.硝酸银溶液.
3.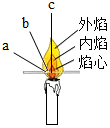 为了探究蜡烛燃烧的现象,做了表中的实验,请你帮忙完成实验报告的内容:
为了探究蜡烛燃烧的现象,做了表中的实验,请你帮忙完成实验报告的内容:
 为了探究蜡烛燃烧的现象,做了表中的实验,请你帮忙完成实验报告的内容:
为了探究蜡烛燃烧的现象,做了表中的实验,请你帮忙完成实验报告的内容:| 实验步骤 | 实验现象 | 结论 |
| 点燃蜡烛,将一根火柴横在火焰上方片刻; | 火柴梗的a(填“a”、“b”或“c”)处最先碳化. | 蜡烛火焰的外焰温度最高. |
| 将一只干冷的烧杯罩在火焰上方; | 烧杯内壁出现水雾. | 说明蜡烛燃烧生成了水. |
| 将一只内壁附有澄清石灰水的烧杯罩在火焰上方. | 烧杯内壁有白色固体生成 | 说明蜡烛燃烧还生成二氧化碳. 蜡烛燃烧的文字表达式为:石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳. |
13.化学反应前后肯定没有变化的是( )
①原子的数目
②分子的数目
③元素的种类
④参加反应各物质的质量总和
⑤物质的种类
⑥原子的种类.
①原子的数目
②分子的数目
③元素的种类
④参加反应各物质的质量总和
⑤物质的种类
⑥原子的种类.
| A. | ①③⑤ | B. | ②④⑥ | C. | ①②④⑥ | D. | ①③④⑥ |
17.下列关于实验现象的描述,正确的是( )
| A. | 镁条在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 磷在氧气中燃烧,产生大量白雾 | |
| C. | 蜡烛在氧气里燃烧生成二氧化碳和水,并放出热量 | |
| D. | 木炭在氧气中燃烧发出白光,并放出热量 |
18.含碳的物质是化学中最大的家族,你了解这一家族吗,你认为下列关于碳及其氧化物的说法中,正确的是( )
| A. | 金刚石很硬、石墨很软,化学性质不同 | |
| B. | CO2不能供给呼吸,能使人窒息死亡,所以二氧化碳是一种有毒气体 | |
| C. | CO有可燃性,可用作燃料 | |
| D. | CO2能用来灭火,只利用了二氧化碳既不能够燃烧也不支持燃烧的化学性质 |
