题目内容
18.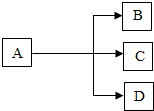 A、B、C、D都是初中化学常见的物质,它们存在如图所示的关系(反应条件均为加热)
A、B、C、D都是初中化学常见的物质,它们存在如图所示的关系(反应条件均为加热)(1)若A为绿色固体,C为黑色固体,则C为CuO(填化学式)
(2)若A为白色固体,是一种常见化肥,产生的B气体有刺激性气味,则B为NH3(填化学式)
(3)若A为紫黑色固体,C为气体,则C可以用带火星的木条来检验,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
分析 框图式分解反应,(1)若A为绿色固体,C为黑色固体,可知是碱式碳酸铜分解产生的氧化铜;
(2)若A为白色固体,是一种常见化肥,产生的B气体有刺激性气味,因此是铵态氮肥分解产生的氨气;
(3)若A为紫黑色固体,C为气体,因此是高锰酸钾分解产生的氧气,据此完成相关的问题.
解答 解:(1)若A为绿色固体,C为黑色固体,可知是碱式碳酸铜分解产生的氧化铜;故填:CuO;
(2)若A为白色固体,是一种常见化肥,产生的B气体有刺激性气味,因此是铵态氮肥分解产生的氨气;故填:NH3;
(3)若A为紫黑色固体,C为气体,因此是高锰酸钾分解产生的氧气,氧气能使带火星的木条复燃,故填:带火星的木条;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 本题为框图式物质推断题,完成此题的关键是根据题干叙述找准解题的突破口,直接得出有关物质的化学式,然后顺推或逆推得出有关物质的化学式.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
6.下列化学方程式能正确表示所述内容的是( )
| A. | 生产汽水:CO2+H2O=H2CO3 | |
| B. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| C. | 湿法炼铜:2Fe+3CuSO4=Fe2(SO4)3+3Cu | |
| D. | 除水垢时铝壶不能用稀盐酸长时间浸泡:Al+2HCl=AlCl3+H2↑ |
13.如图是A、B、C三种固体的溶解度曲线,下列分析正确的是( )


| A. | 50℃时,把45gA物质放入50g水中能得到95g溶液 | |
| B. | 升温可使接近饱和的C物质溶液变成饱和溶液 | |
| C. | 从A、B的混合物中提纯A应采用蒸发结晶法 | |
| D. | 三物质的饱和溶液从20℃升温到50℃后,A的溶质质量分数最大 |
3. 关于如图所示实验,下列说法错误的是( )
关于如图所示实验,下列说法错误的是( )
 关于如图所示实验,下列说法错误的是( )
关于如图所示实验,下列说法错误的是( )| A. | 试管1中气体能燃烧 | B. | 该实验可用于探究水的组成 | ||
| C. | 与试管2相连的是电源正极 | D. | 试管1和试管 2中气体质量比为2:1 |
8.溶解是生活中常见的现象,不同物质在水中的溶解能力不同.下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水).
(1)从NaCl溶液中得到NaCl晶体的方法是蒸发.
(2)现有20℃时质量分数为10%硝酸钾溶液,此溶液不是(填“是”或“不是”)饱和溶液,原因是20℃时KNO3饱和溶液的质量分数为$\frac{31.6g}{100g+31.6g}×$100%=24%>10%.若将20℃时100g 10%的KNO3溶液转化为饱和溶液,应采取的合理措施为在溶液中加入18.44g硝酸钾.(若是饱和溶液,此空可不作答)
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.现将20g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为30g.完成上述实验需要的仪器有ACE(填序号).

| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)现有20℃时质量分数为10%硝酸钾溶液,此溶液不是(填“是”或“不是”)饱和溶液,原因是20℃时KNO3饱和溶液的质量分数为$\frac{31.6g}{100g+31.6g}×$100%=24%>10%.若将20℃时100g 10%的KNO3溶液转化为饱和溶液,应采取的合理措施为在溶液中加入18.44g硝酸钾.(若是饱和溶液,此空可不作答)
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.现将20g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为30g.完成上述实验需要的仪器有ACE(填序号).

 家里开水没有了,小小准备烧一些开水.
家里开水没有了,小小准备烧一些开水.