题目内容
8.工业上用磁铁矿石炼铁,其主要反应原理为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.(1)四氧化三铁中铁元素和氧元素的原子个数比为3:4;
(2)用100t含四氧化三铁58%的磁铁矿石,理论上能炼出纯铁的质量是多少(要求根据化学方程式进行计算)?
分析 (1)根据化学式的意义分析回答;
(2)由磁铁矿石的质量、四氧化三铁的质量分数,根据磁铁矿石炼铁的化学方程式可以列式计算出炼出纯铁的质量.
解答 解:(1)由四氧化三铁化学式的意义可知,铁元素和氧元素的原子个数比为3:4;
(2)100 t该磁铁矿石中Fe3O4的质量为:100 t×58%=58t
设理论上能炼出纯铁的质量为x
Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2
232 168
58t x
$\frac{232}{168}=\frac{58t}{x}$ 解得:x=42t
答:理论上能炼出纯铁的质量是42t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.铜、镁、锌三种金属的活动性由强到弱的顺序为:镁>锌>铜,
为了验证这三种金属的活动性顺序,小阳、小娟、小华各设计了一个探究实验的方案.
(1)小阳所选择的试剂是:MgSO4溶液、Zn、CuSO4溶液.
(2)小娟通过实验也成功地得出了结论,她所选的试剂可能为:Mg、ZnCl2、Cu.请你写出实验过程中发生的化学方程式:Mg+ZnCl2=Zn+MgCl2.
(3)小华说,他用一种试剂稀盐酸分别和这三种金属反应,也能得出实验结论,他完成该实验的依据是:金属与酸能否反应以及反应的剧烈程度可以判断出金属的活泼性,金属越活泼,反应越剧烈.
为了验证这三种金属的活动性顺序,小阳、小娟、小华各设计了一个探究实验的方案.
(1)小阳所选择的试剂是:MgSO4溶液、Zn、CuSO4溶液.
| 实验操作 | 实验现象 |
| 1、将打磨过的Zn片插入MgSO4溶液中 | 无明显现象 |
| 2、将打磨过的Zn片插入CuSO4溶液中 | 锌表面有红色物质析出,溶液由蓝色变为无色 |
(3)小华说,他用一种试剂稀盐酸分别和这三种金属反应,也能得出实验结论,他完成该实验的依据是:金属与酸能否反应以及反应的剧烈程度可以判断出金属的活泼性,金属越活泼,反应越剧烈.
19.关于二氧化碳性质的叙述错误的是( )
| A. | 有毒性 | B. | 可溶于水 | C. | 密度比空气大 | D. | 能与碱溶液反应 |
16.下列物质的俗称、化学式及用途均正确的是( )
| A. | 二氧化碳:干冰、CO、人工降雨 | |
| B. | 氢氧化钠:纯碱、NaOH、作灭火剂 | |
| C. | 甲烷:沼气、CH2、用作燃料 | |
| D. | 氢氧化钙:熟石灰、Ca(OH)2、改良酸性土壤 |
13.将N2、CO、CO2的混合气体依次通入足量氢氧化钠溶液和灼热的氧化铜后,再通入浓硫酸,最后剩余的气体主要是( )
| A. | N2、CO2 | B. | N2 | C. | CO2 | D. | N2、H2O、CO2 |
17.“铁强化酱油”中的“铁”是指( )


| A. | 原子 | B. | 分子 | C. | 单质 | D. | 元素 |

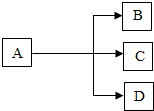 A、B、C、D都是初中化学常见的物质,它们存在如图所示的关系(反应条件均为加热)
A、B、C、D都是初中化学常见的物质,它们存在如图所示的关系(反应条件均为加热)