题目内容
20.粗盐中含有难溶性杂质和多种可溶性杂质(氯化镁、氯化钙等).某同学为了提纯粗盐,设计了如图所示的实验方案:(友情提示:碳酸镁微溶于水)
(1)用化学方程式回答,步骤②的主要目的是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(2)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种就能将两种可溶性杂质除去,你认为这种方法不可行(选填“可行”或“不可行”),理由是碳酸镁、氢氧化钙都是微溶性的,只用任意一种试剂就会生成一种杂质生成微溶物而不能全部除去.
(3)有同学认为原实验方案不完善,做出这种评价的依据是在除去氯化镁和氯化钙的同时又引入了新的杂质氢氧化钠和碳酸钠.
(4)为了完善原实验方案,你的做法是向溶液A中逐滴过量稀盐酸.
分析 (1)加入氢氧化钠的目的是使氯化镁转化为成沉淀,据此写出反应的化学方程式;
(2)根据氢氧化钠、碳酸钠与分别与氯化镁、氯化钙反应生成的碳酸镁、氢氧化钙的溶解性分析;
(3)根据除杂质的原则不能再引入杂质分析回答;
(4)根据在A中含有的杂质分析回答.
解答 解:(1)由提纯粗盐的过程可知,步骤②加入氢氧化钠的目的是除去氯化镁,化学方程式:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(2)如果只用氢氧化钠溶液和碳酸钠溶液中任意一种去除两种可溶性杂质.由于生成的碳酸镁或氢氧化钙是微溶的,只用任意一种试剂就会生成一种杂质生成微溶物而不能全部除去,就会有一种微溶性的杂质混在食盐中,这种方法是不可行的;
(3)在用氢氧化钠溶液和碳酸钠除氯化镁、氯化钙杂质时,又引入了新的杂质氢氧化钠和碳酸钠,所以原实验方案不完善;
(4)由于在A溶液中含有氢氧化钠和碳酸钠杂质,为了完善原实验方案除去杂质,做法是:向溶液A中加入过量稀盐酸.
故答案为:(1)MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(2)不可行,碳酸镁或氢氧化钙是微溶的,只用任意一种试剂就会生成一种杂质微溶物而不能全部除去;
(3)在除去氯化镁和氯化钙的同时又引入了新的杂质氢氧化钠和碳酸钠;
(4)向溶液A中加入过量稀盐酸.
点评 本题综合考查了粗盐的提纯及除杂质的方法,明确步骤,会对误差进行分析,除杂过程中,要根据杂质的种类和性质判断应该选择的试剂,并且掌握过量试剂的除去方法.

练习册系列答案
相关题目
10.如图是固体甲、乙的溶解度曲线图,下列说法正确的是( )


| A. | 将甲、乙两物质的饱和溶液从20℃升到50℃,溶质质量分数大小为:甲>乙 | |
| B. | 甲、乙两物质的溶解度都随温度升高而减小 | |
| C. | 用降温结晶的方法可除去混在甲中的乙物质 | |
| D. | 20℃时,可配制质量分数为30%的乙物质溶液 |
11.用过氧化氢和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,据此填表.
| 项目 | 反应物 | 生成物 | |
| H2O2 | H2O | O2 | |
| 质量比 | 68 | 36 | 32 |
| A | 34g | 18g | 16g |
| B | 17g | 9g | 8g |
9. 核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等原子及一些粒子和射线,同时释放大量的能量,这些能量可用于驱动,汽轮机发电,锶元素在元素周期表中显示的信息和锶原子的结构示意图如图所示,下列说法正确的是( )
核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等原子及一些粒子和射线,同时释放大量的能量,这些能量可用于驱动,汽轮机发电,锶元素在元素周期表中显示的信息和锶原子的结构示意图如图所示,下列说法正确的是( )
 核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等原子及一些粒子和射线,同时释放大量的能量,这些能量可用于驱动,汽轮机发电,锶元素在元素周期表中显示的信息和锶原子的结构示意图如图所示,下列说法正确的是( )
核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等原子及一些粒子和射线,同时释放大量的能量,这些能量可用于驱动,汽轮机发电,锶元素在元素周期表中显示的信息和锶原子的结构示意图如图所示,下列说法正确的是( )| A. | Sr为非金属元素 | B. | 锶原子的中子数是38 | ||
| C. | 锶原子的质量为87.62g | D. | 锶在化学反应中易失去2个电子 |
10.下列说法不正确的是( )
| A. | 用灼烧法可以鉴别羊毛和合成纤维 | |
| B. | 催化剂一定能加快化学反应的速率 | |
| C. | 碳酸氢钠是焙制糕点的发酵粉的主要成分之一 | |
| D. | 洗涤剂具有乳化功能可除去油污 |
 点燃两支蜡烛,分别入在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.
点燃两支蜡烛,分别入在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.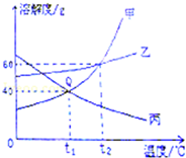 如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题.
如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题.