题目内容
20.已知向某碳酸盐溶液中滴加稀盐酸至过量,生成气体的质量(m)与加入盐酸的体积(V)的关系如图一所示.现将1.12g KOH和1.38g K2CO3混合并配成溶液,向其中滴加稀盐酸,图二是甲、乙、丙三位同学分别绘制的产生气体的质量(m)与稀盐酸的体积(V)的关系的示示意图.下面判断正确的是( )
| A. | 甲图正确 | B. | 乙图正确 | C. | 丙图正确 | D. | 无法判断 |
分析 对KOH和K2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钾与盐酸的中和反应,再发生碳酸钾与盐酸的反应生成碳酸氢钾和氯化钾,最后发生碳酸氢钾与盐酸反应才有二氧化碳气体生成,利用物质的量的关系并结合图象即可解答.
解答 解:KOH和K2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钾与盐酸的中和反应,再发生碳酸钾与盐酸的反应生成碳酸氢钾和氯化钾,最后发生碳酸氢钾与盐酸反应才有二氧化碳气体生成,由化学方程式
KOH+HCl=KCl+H2O;
56 36.5
1.12g 0.73g
HCl+K2CO3=KHCO3+KCl,
36.5 138 100
0.365g 1.38g 1.00g
KHCO3+HCl=KCl+H2O+CO2↑,
100 36.5
1.00g 0.365g
所以氢氧化钾与盐酸的中和反应,碳酸钾与盐酸的反应所用盐酸质量与碳酸氢钾与盐酸反应所用盐酸质量的为(0.73g+0.365g):0.365g=3:1.所以图象如图丙所示.
故选C.
点评 此题考查了元素化合物性质、图象计算等,解答此题关键是明确向碳酸钠溶液中滴加盐酸的反应是分步进行的,首先发生的是HCl+K2CO3=KHCO3+KCl;进行完全后,再发生:KHCO3+HCl=KCl+H2O+CO2↑.

练习册系列答案
相关题目
10.下列各组中的两种物质,能通过同一个化学反应得到的是( )
| A. | 氯化钠和二氧化碳 | B. | 铁和硝酸银 | ||
| C. | 碳酸钙和硝酸 | D. | 碳酸钠和氢氧化钙 |
15.2015年8月12日23:30左右,位于天津滨海新区塘沽开发区的天津东疆保税港区瑞海国际物流有限公司所属危险品仓库发生爆炸.截至2015年9月11日下午3点,天津港“8•12”爆炸共发现遇难者总人数升至165人,仍有8人失联.其中公安消防人员24人,天津港消防人员75人,民警11人,其他人员55人.下列生活中处理火灾事故的方法中正确的是( )
| A. | 家用电器着火,用水扑灭 | |
| B. | 档案资料着火,可用液态二氧化碳扑灭 | |
| C. | 室内起火,迅速打开所有门窗通风 | |
| D. | 高层楼房失火时,要乘电梯迅速撤离 |
7.1303班同学在学习了“二氧化锰在过氧化氢溶液分解中起催化作用”后,想探究氧化铁能否在过氧化氢溶液分解中起到催化作用,请你一起参与他们的探究过程.
【提出问题】氧化铁能否在过氧化氢溶液分解中起到催化作用?
【设计实验】
【分析实验】
(1)H2O2溶液在常温下可以分解(填“可以分解”或“不可以分解”)放出氧气.
(2)写出氧化铁催化过氧化氢溶液分解的化学方程式2H2O2$\frac{\underline{\;氧化铁\;}}{\;}$2H2O+O2↑.
【交流讨论】有的同学认为只有上述三个实验还不能证明Fe2O3能作过氧化氢溶液分解反应的催化剂,还要补充如下探究实验.
实验目的:探究化学反应前后氧化铁的质量是否相等.
实验步骤:①待反应结束,将试管里的物质进行过滤,洗涤,干燥,称量.
②对比反应前后氧化铁的质量.
【预期结论】氧化铁能在过氯化氢溶液分解中起到催化作用
【深入研究】氧化铁与二氧化锰都能做过氧化氢的催化剂.哪一种催化效果更好?
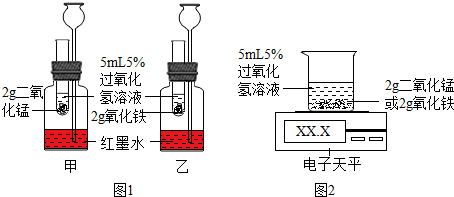
【定性研究】如图1,室温下通过比较两试管中产生气泡的快慢来定性两者的催化效果.假如二氧化锰的催化效果明显更好.两支长颈漏斗产生的现象的不同之处是甲装置中长颈漏斗的液面比乙装置的高.
【定量研究】如图2,室温下通过比较相同时间内天平读数差值大小来定量两者的催化效果.

【提出问题】氧化铁能否在过氧化氢溶液分解中起到催化作用?
【设计实验】
| 实验步骤 | 实验现象 | |
| 实验1 | 在试管中加入少量的H2O2溶液,然后将带火星的木条伸入试管中,观察现象. | 木条不复燃 |
| 实验2 | 在实验1的试管中加入ag的氧化铁,然后将带火星的木条伸入试管中,观察现象. | 木条复燃 |
| 实验3 | 待实验2试管中没有气泡产生后,再加入过氧化氢溶液,然后将带火星的木条伸入试管中,观察现象.反复多次实验. | 木条均复燃 |
(1)H2O2溶液在常温下可以分解(填“可以分解”或“不可以分解”)放出氧气.
(2)写出氧化铁催化过氧化氢溶液分解的化学方程式2H2O2$\frac{\underline{\;氧化铁\;}}{\;}$2H2O+O2↑.
【交流讨论】有的同学认为只有上述三个实验还不能证明Fe2O3能作过氧化氢溶液分解反应的催化剂,还要补充如下探究实验.
实验目的:探究化学反应前后氧化铁的质量是否相等.
实验步骤:①待反应结束,将试管里的物质进行过滤,洗涤,干燥,称量.
②对比反应前后氧化铁的质量.
【预期结论】氧化铁能在过氯化氢溶液分解中起到催化作用
【深入研究】氧化铁与二氧化锰都能做过氧化氢的催化剂.哪一种催化效果更好?
【定性研究】如图1,室温下通过比较两试管中产生气泡的快慢来定性两者的催化效果.假如二氧化锰的催化效果明显更好.两支长颈漏斗产生的现象的不同之处是甲装置中长颈漏斗的液面比乙装置的高.
【定量研究】如图2,室温下通过比较相同时间内天平读数差值大小来定量两者的催化效果.
4.检验糖尿病人的尿液,要配制8%的硫酸铜溶液200g.下列配制过程中正确的是( )
| A. | 只需托盘天平和量筒两种仪器 | |
| B. | 砝码放在左盘上,称取16g无水硫酸铜 | |
| C. | 用量筒量取184mL的水 | |
| D. | 把无水硫酸铜倒入量筒中搅拌溶解 |
5.在氧气中燃烧,会产生浓厚白烟的是( )
| A. | 红磷 | B. | 木炭 | C. | 硫磺 | D. | 铁丝 |