题目内容
18.人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用.请回答下列问题:(1)根据如图金属应用实例推断,金属具有的物理性质有导热性、导电性(至少答两点);

(2)微型化录音录像的高性能带中磁粉主要材料之一是化学组成相当于CoFe2O4的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,则铁元素的化合价为+3;
(3)在硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定量金属铝,反应停止后过滤,滤液仍为蓝色.
①滤液中一定含有的溶质是Al(NO3)3、Cu(NO3)2、Mg(NO3)2(写化学式)
②请写出该过程中一定发生的反应的化学方程式Al+3AgNO3═3Ag+Al(NO3)3.
③若向所得固体上滴加稀盐酸,则一定没有(填“一定有”、“可能有”或“一定没有”)气泡产生.
分析 (1)根据金属的物理性质进行分析;
(2)根据在化合物中正负化合价代数和为零,结合CoFe2O4的化学式进行解答本题;
(3)根据四种金属活动性由强到弱的顺序:镁>铝>铜>银,当把铝粉加入到硝酸镁、硝酸铜和硝酸银的混合溶液中时,银首先被置换出来,在银完全置换后,铜才能被置换出来,铝不会与硝酸镁反应,由反应停止后过滤,滤液仍为蓝色,说明滤液中含有硝酸铜,铝可能没有置换出铜,有可能置换出部分铜进行分析.
解答 解:(1)物理性质:物质不需要发生化学变化就表现出来的性质,如:颜色、状态、气味、硬度、熔点、沸点、密度等,金属可以制作电线说明金属具有良好的导电性,可以制作热水壶说明金属具有良好的导热性,可以拉成丝说明金属具有良好的延展性;
(2)若钴和铁元素的化合价相同时,即都为+2价时,则钴和铁的化合价的和为:(+2)+(+2)×2+(-2)×4≠0;都为+3价时,钴和铁的化合价的和为:(+3)+(+3)×2+(-2)×4≠0;则都不符合要求,所以化合物中Co和Fe的化合价不同;
因此Co、Fe的化合价可能为+2、+3价或+3、+2价;
若Co的化合价为+3,Fe的化合价为+2时,钴和铁的化合价的和为:(+3)+(+2)×2+(-2)×4≠0,不符合要求;
若Co的化合价为+2,Fe的化合价为+3,钴和铁的化合价的和为:(+2)+(+3)×2+(-2)×4=0,符合要求;
(3)四种金属活动性由强到弱的顺序:镁>铝>铜>银,当把铝粉加入到硝酸镁、硝酸铜和硝酸银的混合溶液中时,银首先被置换出来,在银完全置换后,铜才能被置换出来,铝不会与硝酸镁反应,由反应停止后过滤,滤液仍为蓝色,说明滤液中含有硝酸铜,铝可能没有置换出铜,有可能置换出部分铜,所以
①滤液中一定含有的溶质是:Al(NO3)3、Cu(NO3)2、Mg(NO3)2;
②该过程中一定发生的反应是铝和硝酸银反应生成硝酸铝和银,化学方程式为:Al+3AgNO3═3Ag+Al(NO3)3;
③通过分析可知,铝没有剩余,所以向所得固体上滴加稀盐酸,则一定没有气泡产生.
故答案为:(1)导电性、导热性;
(2)+3;
(3)①Al(NO3)3、Cu(NO3)2、Mg(NO3)2;
②Al+3AgNO3═3Ag+Al(NO3)3;
③一定没有.
点评 本题综合性较强,主要考查了金属的性质,是一道不错的题目,掌握金属材料的范畴并能灵活运用是正确解答此类题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | 表示甲烷与氧气在点燃条件下反应生成水和二氧化碳 | |
| B. | 反应前和反应后的分子数目不变 | |
| C. | 参加反应的甲烷与氧气的质量比为1:4 | |
| D. | 参加反应的氧气与生成的二氧化碳的分子个数比为1:2 |
| A. | 在酱油中加入铁强化剂以补充铁元素 | |
| B. | 食用酒精和工业酒精的主要成分相同,都可以饮用 | |
| C. | 低血糖病症发作时,吃馒头比喝葡萄糖水见效快 | |
| D. | 防止“碘-131”核辐射,吃大量的加碘盐 |
【实验用品】pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液.
【猜想与假设】反应后溶液总溶质的可能组成成分.
猜想一:硫酸钠
猜想二:硫酸钠、碳酸氢钠
猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成如表实验现象中的空格.
| 实验方案 | A | B | C | D |
| 实验操作 | 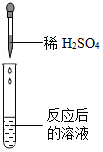 | 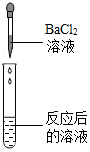 | 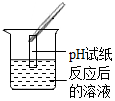 |  |
| 实验现象 | 无气泡产生 | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH<7 | 有气泡产生 |
| 实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
【评价反思】
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显错误是:C实验中将pH试纸直接浸入待测液.
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由氯化钡与硫酸钠也能反应产生白色沉淀.
【总结提高】依据所给实验用品,设计不同的方案确认猜想三是正确的,请你写出你的实验方案取少量氧化铜粉末于试管中,加入足量反应后的溶液,若氧化铜溶解,溶液变蓝,则猜想三正确.
| A. |  鲫鱼汤 | B. |  炸臭豆腐 | C. |  烤辣椒 | D. |  南京肉馅小龙包 |
| A. | 碳酸钠10g、碳酸钙10g | B. | 铁5.6g、锌5.6g | ||
| C. | 铁8.0g、氧化铜8.0g | D. | 碳酸钙10g、碳酸镁10g |
 铅蓄电池在生产、生活中使用广泛.其构造示意图如图,回答下列问题:
铅蓄电池在生产、生活中使用广泛.其构造示意图如图,回答下列问题: 2017年4月7日,哈佳铁路哈尔滨特大桥跨民主堤连续梁主跨合龙.这是特大桥今年开春复工以来合龙的首联连续梁.目前,特大桥五联连续梁已合龙两联,剩余的计划在下月底前合龙,为新建哈佳铁路2018年投用奠定基础.
2017年4月7日,哈佳铁路哈尔滨特大桥跨民主堤连续梁主跨合龙.这是特大桥今年开春复工以来合龙的首联连续梁.目前,特大桥五联连续梁已合龙两联,剩余的计划在下月底前合龙,为新建哈佳铁路2018年投用奠定基础.