题目内容
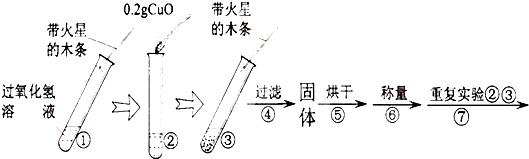
将木炭和氧化铜的粉末混合物15g,加热一段时间后,冷却称量固体的质量为12.8g.求参加反应的氧化铜的质量?(相对原子质量:Cu-64,O-16,C-12).
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:碳还原氧化铜生成铜和二氧化碳;固体减少的质量即生成的二氧化碳的质量,据此根据反应的化学方程式列式计算出参加反应的氧化铜的质量.
解答:解:由质量守恒定律,固体减少的质量即生成的二氧化碳的质量,则生成二氧化碳气体的质量为15g-12.8g=2.2g.
设参加反应的氧化铜的质量是x,
C+2CuO
2Cu+CO2↑
160 44
x 2.2g
=
x=8g.
答:参加反应的氧化铜的质量为8g.
设参加反应的氧化铜的质量是x,
C+2CuO
| ||
160 44
x 2.2g
| 160 |
| 44 |
| x |
| 2.2g |
答:参加反应的氧化铜的质量为8g.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
下列关于实验现象的描述,错误的是( )
| A、镁条在氧气中燃烧,火星四射,生成黑色固体 |
| B、磷在氧气中燃烧,产生大量白烟 |
| C、硫在氧气中燃烧,火焰呈明亮的蓝紫色,生成有刺激性气味的气体 |
| D、木柴在氧气中燃烧发出白光而在空气中燃烧则呈红色的灼热状 |
物质在空气中发生缓慢氧化、燃烧的共同点是( )
| A、都放出热量 | B、都生成气体 |
| C、都有响声 | D、都发光 |
下列实验现象描述正确的是( )
| A、磷在空气中燃烧,产生大量的白雾,放出大量的热 |
| B、硫在空气中燃烧,产生淡蓝色火焰,生成刺激性气味气体,放热 |
| C、碳在空气中燃烧,产生红色火焰,放出大量的热 |
| D、蜡烛在氧气中燃烧,生成水和二氧化碳 |
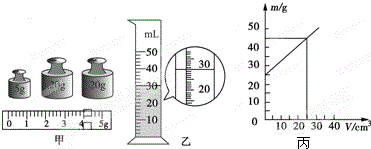 为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下:
为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下: