题目内容
18.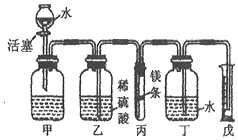 某科学兴趣小组的同学欲在常温、常压下,用质量为m的镁与足量的稀硫酸反应,测定镁的相对原子质量.利用如图所示的装置进行实验,盛放镁条的隔板有小孔,图中固定装置已略去,充分反应后,测得生成氢气的体积为V.已知本实验条件下,氢气的密度为ρ;镁与稀硫酸的反应为放热反应,
某科学兴趣小组的同学欲在常温、常压下,用质量为m的镁与足量的稀硫酸反应,测定镁的相对原子质量.利用如图所示的装置进行实验,盛放镁条的隔板有小孔,图中固定装置已略去,充分反应后,测得生成氢气的体积为V.已知本实验条件下,氢气的密度为ρ;镁与稀硫酸的反应为放热反应,反应化学方程式:Mg+H2SO4═MgSO4+H2↑.
(1)实验开始时,能使乙装置中稀硫酸进入丙装置的具体操作是打开活塞,使水进入甲中.
(2)实验测得的镁相对原子质量为$\frac{2m}{ρV}$.
(3)关于该实验,有如下说法,其中正确的有①③.(可多选)
①连接仪器后,要先检查装置的气密性
②当丙中无气泡产生,立即读取戊量筒中水的体积,即反应生成氢气的体积
③装置中的空气对实验结果无影响
④利用该实验原理,还可以测定铜的相对原子质量.
分析 (1)实验开始时,能使乙装置中稀硫酸进入丙装置的具体操作是打开活塞,使水进入甲中,甲中气压增大,导致部分气体进入乙中,乙中气压增大,把乙装置中稀硫酸排入丙装置;
(2)根据反应的化学方程式及其氢气的体积、密度等可以计算镁的相对原子质量;
(3)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
气体压强随着温度升高而增大.
解答 解:(1)实验开始时,能使乙装置中稀硫酸进入丙装置的具体操作是:打开活塞,使水进入甲中,甲中气压增大,导致部分气体进入乙中,乙中气压增大,把乙装置中稀硫酸排入丙装置.
故填:打开活塞,使水进入甲中,甲中气压增大,导致部分气体进入乙中,乙中气压增大,把乙装置中稀硫酸排入丙装置.
(2)设镁的相对原子质量为x,
Mg+H2SO4═MgSO4+H2↑,
x 2
m ρV
$\frac{x}{m}$=$\frac{2}{ρV}$,
x=$\frac{2m}{ρV}$,
故填:$\frac{2m}{ρV}$.
(3)①连接仪器后,要先检查装置的气密性,该选项说法正确;
②当丙中无气泡产生,不能立即读取戊量筒中水的体积,这是因为反应放热,导致气球的体积膨胀,应该冷却至室温再读取戊量筒中水的体积,该选项说法不正确;
③装置中的空气对实验结果无影响,这是因为生成多少体积的氢气,就有多少体积的水排入量筒中,该选项说法正确;
④利用该实验原理,不能测定铜的相对原子质量,这是因为铜不能和稀硫酸反应.
故选:①③.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | 硝酸铵溶于水,溶液温度升高 | |
| B. | 灼烧羊毛线,闻到一股烧焦羽毛的气味 | |
| C. | 用洗洁精洗去餐具上的油污,属于乳化在日常生活中的应用 | |
| D. | 工业上分离液态空气获得氧气,是利用液氧和液氮的沸点不同 |
| A. | 氮气的化学性质稳定可作保护气 | |
| B. | 厨房内燃气泄漏时应立即打开排气扇 | |
| C. | 工业上用汽油或烧碱溶液等清洗油污 | |
| D. | 购物时使用棉布袋有利于减少“白色污染” |
| A. | 化合反应、分解反应 | B. | 化合反应、分解反应、置换反应 | ||
| C. | 置换反应、复分解反应 | D. | 化合反应、分解反应、复分解反应 |
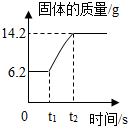 用“红磷燃烧”法测定空气中氧气含量实验中,密闭容器中固体变化如图所示.
用“红磷燃烧”法测定空气中氧气含量实验中,密闭容器中固体变化如图所示.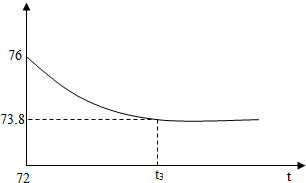 某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定 该样品中碳酸钙的质量,他们将一块样品敲打粉碎后,取出 6g 放入质量为 20g 的烧杯 中,然后加入稀盐酸,用玻璃棒搅拌至不再产生气泡为止,共消耗掉盐酸的质量为 50g. 反应所需时间和烧杯及其所盛物质的总质量变化如
某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定 该样品中碳酸钙的质量,他们将一块样品敲打粉碎后,取出 6g 放入质量为 20g 的烧杯 中,然后加入稀盐酸,用玻璃棒搅拌至不再产生气泡为止,共消耗掉盐酸的质量为 50g. 反应所需时间和烧杯及其所盛物质的总质量变化如