题目内容
19.实验室常用下列装置制取气体,请你根据所学知识回答下列问题.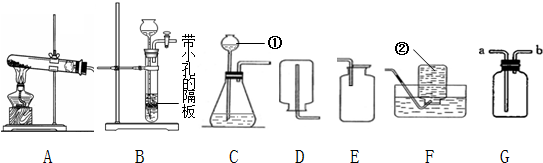
(1)写出编号所指仪器的名称:①长颈漏斗;②集气瓶.
(2)以上装置图中有一处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:E装置的导管应该伸入集气瓶底部.
(3)小李在实验室中选择上述装置中的A和F进行组装制取氧气,其反应的化学方程:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)西气东输所输送的气体是天然气,天然气的主要成分是甲烷,是一种极难溶解于水的气体,密度小于空气的密度,实验室常用加热无水醋酸钠和碱石灰两种固体混合物的方法来制取.发生装置选择A,选择理由是反应物是固体和液体,反应条件需要加热,用G装置收集CH4,则CH4应从导管口b通入(填a或b).
(5)装置B、C都可以用来制取氢气中的气体,比较这两个装置的不同,指出B装置的一个突出优点可以控制反应的发生和停止.
(6)在“G”装置中盛装适量的浓硫酸后可用来除去混合气体中的水蒸气.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据排空气法收集气体时,需要将导管伸入试管底部进行分析;
(3)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(4)根据发生装置选择A制取气体的反应物是固体和液体,反应条件需要加热,甲烷密度比空气小进行分析;
(5)根据B装置可以利用压强差实现固体和液体分离进行分析;
(6)根据浓硫酸有吸水性进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗,②是集气瓶;
(2)排空气法收集气体时,需要将导管伸入试管底部;
(3)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)发生装置选择A制取气体的反应物是固体和液体,反应条件需要加热,甲烷密度比空气小,所以用G装置收集CH4,则CH4应从导管口b通入;
(5)B装置可以利用压强差实现固体和液体分离,所以B装置的一个突出优点是:可以控制反应的发生和停止;
(6)浓硫酸有吸水性,所以在“G”装置中盛装适量的浓硫酸后可用来除去混合气体中的水蒸气.
故答案为:(1)长颈漏斗,集气瓶;
(2)E装置的导管应该伸入集气瓶底部;
(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)反应物是固体和液体,反应条件需要加热,b;
(5)可以控制反应的发生和停止;
(6)水蒸气.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
9.生活即化学,生活中有很多的变化都蕴含着化学原理,下列变化属于化学变化的是( )
| A. | 汽油挥发 | B. | 燃放烟花 | ||
| C. | 活性炭吸附冰箱内的异味 | D. | 分离液态空气制取氧气 |
7.向一定质量的硫酸铜溶液中加入一定质量的铁粉,反应一段时间后,溶液的质量( )
| A. | 变小 | B. | 变大 | C. | 不变 | D. | 无法确定 |
14.下列基本实验操作正确的是( )
| A. |  液体读数 | B. |  摆放试管 | C. |  洗涤试管 | D. |  倾倒液体 |
11.氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,氢氟酸与玻璃发生的反应可以表示为SiO2+4HF═X↑+2H2O,关于物质X的组成,下列说法正确的是( )
| A. | 可能含有氢元素 | B. | 一定含有硅元素、氟元素 | ||
| C. | 可能含有氧元素 | D. | X是一种氧化物 |
8.某学校化学兴趣小组的同学们在实验室发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.物为了弄清楚白色粉末的成分形成原因,他们进行了如下探究:
【提出问题】白色粉末的成分的什么?
【做出猜想】①甲同学认为可能是CaCO3:原因是石灰水与空气中的CO2反应.
②乙同学认为可能是氢氧化钙:原因是溶剂蒸发,石灰水中的溶质结晶析出.
③丙同学认为还可能是碳酸钙和氢氧化钙.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是氢氧化钙微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
由上述实验可知,白色粉末成分的猜想③同学是正确的.
【拓展反思】实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl═CaCl2+H2O+CO2↑,或Ca(OH)2+2HCl═CaCl2+2H2O.
【提出问题】白色粉末的成分的什么?
【做出猜想】①甲同学认为可能是CaCO3:原因是石灰水与空气中的CO2反应.
②乙同学认为可能是氢氧化钙:原因是溶剂蒸发,石灰水中的溶质结晶析出.
③丙同学认为还可能是碳酸钙和氢氧化钙.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是氢氧化钙微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取上述试管中的上层溶液,滴加1~2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中含有Ca(OH)2 |
| ②往上述试管残留的白色固体中加入稀盐酸 | 有气泡产生 | 白色粉末中含有碳酸钙 |
【拓展反思】实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl═CaCl2+H2O+CO2↑,或Ca(OH)2+2HCl═CaCl2+2H2O.
