题目内容
11.氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,氢氟酸与玻璃发生的反应可以表示为SiO2+4HF═X↑+2H2O,关于物质X的组成,下列说法正确的是( )| A. | 可能含有氢元素 | B. | 一定含有硅元素、氟元素 | ||
| C. | 可能含有氧元素 | D. | X是一种氧化物 |
分析 根据化学变化前后原子的种类、数目不变,由反应的化学方程式SiO2+4HF═X↑+2H2O,推断反应中生成物X的分子构成,然后确定X物质的化学式,根据化学式判断说法中正确的选项.
解答 解:由反应的化学方程式SiO2+4HF═X↑+2H2O,可知:
反应前 反应后
Si原子 1 0
O原子 2 2
H原子 4 4
F原子 4 0
根据化学变化前后原子的种类、数目不变,可判断物质X的分子由1个Si原子和4个F原子构成,则物质X的化学式可表示为SiF4;物质X由硅、氟两种元素组成,故B正确;物质X中不含H、O元素,不属于氧化物,故A、C、D错误.
故选:B.
点评 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列实验现象的描述符合事实的是( )
| A. | 碳在氧气中燃烧生成二氧化碳 | |
| B. | 将点燃的木条放入盛满二氧化碳的集气瓶中,木条的火焰熄灭 | |
| C. | 铁在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 红磷在氧气中燃烧,生成大量白雾 |
2.下列变化都属于化学变化的是( )
| A. | 汽油挥发、铁生锈 | |
| B. | 燃放烟花、二氧化碳通入澄清石灰水中 | |
| C. | 活性炭吸附冰箱内异味、干冰升华 | |
| D. | 分离液态空气得到氧气、食物腐烂 |
16.下列图示实验操作中,正确的是( )
| A. | 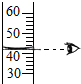 读取液体体积 | B. | 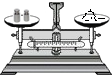 称量固体质量 称量固体质量 | C. | 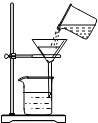 过滤 | D. | 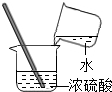 稀释浓硫酸 |
3.小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体开展探究,请你与他们一起进行探究.
提出问题:
这瓶氢氧化钠固体是否变质?
猜想与假设:
氢氧化钠没有变质;该氢氧化钠部分变质;该氢氧化钠全部变质
设计实验:
取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
反思与交流:
(4)久置的氢氧化钠变质的原因是(用化学方程式)CO2+2NaOH=Na2CO3+H2O.
探究与拓展:
(5)为进一步探究氢氧化钠的变质程度,小明称取20克氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产上气泡为止,共消耗稀盐酸100克,反应后称的烧杯中溶液的质量为115.6克,求该样品中碳酸钠的质量分数(要写出计算过程).
提出问题:
这瓶氢氧化钠固体是否变质?
猜想与假设:
氢氧化钠没有变质;该氢氧化钠部分变质;该氢氧化钠全部变质
设计实验:
取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A 于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想(1)不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式)CO2+2NaOH=Na2CO3+H2O.
探究与拓展:
(5)为进一步探究氢氧化钠的变质程度,小明称取20克氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产上气泡为止,共消耗稀盐酸100克,反应后称的烧杯中溶液的质量为115.6克,求该样品中碳酸钠的质量分数(要写出计算过程).
20.下列关于金属的说法正确的是( )
| A. | 人类使用金属铝的年代早于铜、铁 | |
| B. | “真金不怕火炼”表明金的熔点高 | |
| C. | 通过高炉炼得的铁为生铁 | |
| D. | 武德合金的熔点高,可用于制造保险丝 |
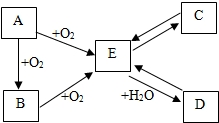 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色固体.其转化关系如图所示: