题目内容
7. 以下为初中化学常见物质,由H、C、O、S、Na、Ca、Fe等元素组成.
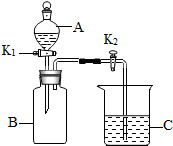
以下为初中化学常见物质,由H、C、O、S、Na、Ca、Fe等元素组成.同学们利用此图做了如下实验(A、B、C中盛放有不同的药品):
【实验1】若将红棕色固体放入B中,打开K1、K2,将A中液体加入B中,关K1,观察到B中溶液变为黄色,一段时间后,盛水的C中导管口有大量气泡冒出,B中溶液变为浅绿色,则B中盛放的物质为生锈的铁,A中液体为稀硫酸.B中发生置换反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
【实验2】若B中集满某纯净气体,打开K1、K2,将A中液体加入B中,关闭K1、K2,充分反应后,打开K2,观察到C中液体进入B中且变浑浊,则B中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
分析 【实验1】根据固体为红棕色滴加液体后溶液先变黄色后产生气体,所以可以考虑生锈的铁与稀酸的反应;
【实验2】根据气体能与A中的液体反应且能使B中的压强减小且产物能与C中的液体反应生成沉淀分析解答.
解答 解:【实验1】根据固体为红棕色滴加液体后溶液先变黄色后产生气体,所以可以考虑生锈的铁与稀酸的反应;该过程是铁锈中的氧化铁先于硫酸反应生成硫酸铁(其溶液呈黄色),铁锈反应完全后,铁能与硫酸反应生成氢气,所以有气泡冒出;
【实验2】根据气体能与A中的液体反应且能使B中的压强减小且产物能与C中的液体反应生成沉淀,故B中的气体是二氧化碳,A中的液体可以是氢氧化钠溶液,两者能够反应生成碳酸钠和水,而C中可以是氢氧化钙的溶液,进入B后碳酸钠能够和氢氧化钙反应生成碳酸钙沉淀,导致溶液变混;化学方程式为:CO2+2NaOH=Na2CO3+H2O,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
故答案为:【实验1】生锈的铁(铁和氧化铁),稀硫酸,Fe+H2SO4═FeSO4+H2↑;
【实验2】CO2+2NaOH═Na2CO3+H2O,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 本题考查了常见物质成分的推断,完成此题,可以依据物质的性质进行.书写反应的化学方程式要注意配平.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.CO和CO2混合气体含碳元素36%,取此混合气体10g,通过足量灼热的CuO后,将气体通过足量的澄清石灰水,得到白色沉淀的质量是( )
| A. | 5g | B. | 10g | C. | 20g | D. | 30g |
16.下列图象与对应选项关系不合理的是( )
| A. | 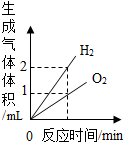 电解水时生成氢气和氧气的体积关系 | |
| B. | 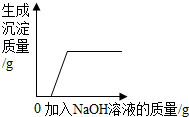 向盐酸和氯化铜的混合物溶液中滴加过量的氢氧化钠溶液 | |
| C. | 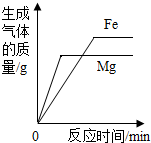 将等质量的镁粉、铁粉分别加入到足量且溶质质量分数相同的稀硫酸中 | |
| D. | 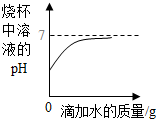 向盛有一定质量稀盐酸的烧杯中不断加水稀释 |
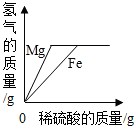

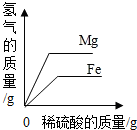

 某化学兴趣小组的同学用如图所示装置进行以下三个实验.
某化学兴趣小组的同学用如图所示装置进行以下三个实验.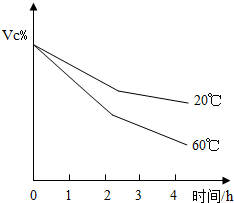 兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.
兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究. 某化学兴趣小组用如右所示装置研究浓盐酸的性质.
某化学兴趣小组用如右所示装置研究浓盐酸的性质.