题目内容
某活动性小组的同学,正在设计实验证明Fe、Cu、Ag三种金属的活动性强弱.化学老师给他们提供如下药品:稀盐酸、铜丝、硝酸银溶液、铁丝、银片、硫酸铜溶液、硫酸亚铁溶液、硫酸锌溶液(仪器任选),让他们从中选择药品设计三种不同的实验方案(每种方案选择的药品最多不超过四种).请你和他们一起探究,帮助他们完成下面的实验报告:
| 方案 | 所选药品 | 实验步骤 | 涉及反应方程式 |
| 1 | |||
| 2 | |||
| 3 |
考点:金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.
解答:解:根据金属活动顺序,Fe>H>Cu>Ag.这是进行分析的基础.下面设计的实验的分析就要结合这个结论来进行.
1、取中间的金属对应的可溶性的盐溶液,其余两种都用单质,Fe、CuSO4溶液、Ag:Fe和CuSO4反应,则Fe>Cu;而Ag和CuSO4不反应,则Cu>Ag.所以可以得出Fe>Cu>Ag.故用2支试管各取少量Cu(NO3)2溶液,分别插入铁丝、银丝,铁丝表面覆盖一层红色铜,银丝表面无变化;
2、取中间的金属的单质,另外两种取对应盐溶液.Cu、FeSO4溶液、AgNO3溶液.可以进行的实验时将铜粉或者铜丝分别插入(或加入)到FeCl2溶液和AgNO3溶液,铜丝遇到FeCl2溶液无明显现象,得出Fe>Cu;遇到AgNO3溶液表面变成白色,溶液也变成蓝色,得出Cu>Ag.所以得出Fe>Cu>Ag.
3、Fe、Cu、AgNO3溶液、稀盐酸:Fe和稀盐酸反应,得出Fe>H.而Cu和Ag均不能与稀盐酸反应,所以Fe>Cu,Fe>Ag.Cu和AgNO3溶液反应,则Cu>Ag.所以可以得出:Fe>Cu>Ag.故用3支试管各取少量HCl,分别插入铁丝、铜丝、银丝,取少量AgNO3溶液,插入铜丝;铁丝表面有气泡产生,铜丝、银丝表面无变化,铜丝表面覆盖一层银白色金属.
故答案为:
1、取中间的金属对应的可溶性的盐溶液,其余两种都用单质,Fe、CuSO4溶液、Ag:Fe和CuSO4反应,则Fe>Cu;而Ag和CuSO4不反应,则Cu>Ag.所以可以得出Fe>Cu>Ag.故用2支试管各取少量Cu(NO3)2溶液,分别插入铁丝、银丝,铁丝表面覆盖一层红色铜,银丝表面无变化;
2、取中间的金属的单质,另外两种取对应盐溶液.Cu、FeSO4溶液、AgNO3溶液.可以进行的实验时将铜粉或者铜丝分别插入(或加入)到FeCl2溶液和AgNO3溶液,铜丝遇到FeCl2溶液无明显现象,得出Fe>Cu;遇到AgNO3溶液表面变成白色,溶液也变成蓝色,得出Cu>Ag.所以得出Fe>Cu>Ag.
3、Fe、Cu、AgNO3溶液、稀盐酸:Fe和稀盐酸反应,得出Fe>H.而Cu和Ag均不能与稀盐酸反应,所以Fe>Cu,Fe>Ag.Cu和AgNO3溶液反应,则Cu>Ag.所以可以得出:Fe>Cu>Ag.故用3支试管各取少量HCl,分别插入铁丝、铜丝、银丝,取少量AgNO3溶液,插入铜丝;铁丝表面有气泡产生,铜丝、银丝表面无变化,铜丝表面覆盖一层银白色金属.
故答案为:
| 方案 | 所选药品 | 实验步骤 | 涉及反应方程式 |
| 1 | Fe、CuSO4溶液、Ag | 2支试管各取少量Cu(NO3)2溶液,分别插入铁丝、银丝,铁丝表面覆盖一层红色铜,银丝表面无变化 | Fe+CuSO4═FeSO4+Cu |
| 2 | Cu、FeSO4溶液、AgNO3溶液 | 2支试管各取少量FeSO4溶液和AgNO3溶液,分别插入铜丝,插入AgNO3溶液表面有银白色物质出现. | Cu+2AgNO3═Cu(NO3)2+2Ag |
| 3 | Fe、Cu、AgNO3溶液、稀盐酸 | 用3支试管各取少量HCl,分别插入铁丝、铜丝、银丝,取少量AgNO3溶液,插入铜丝;铁丝表面有气泡产生,铜丝、银丝表面无变化,铜丝表面覆盖一层银白色金属 |
点评:金属活动的探究实验,可以设计不同的方案,而并非每一个方案都能形成相应结论,这就要求我们认真分析每一个方案,最终选择出合理方案付诸实施.分析时要从已经掌握的金属活动顺序来分析,判断反应是否发生,然后从反应的是否反应以及反应的快慢形成结论,最后归纳出所探究所有金属之间的关系.

练习册系列答案
相关题目
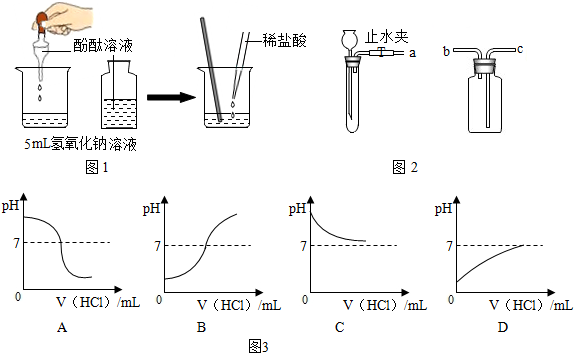
两瓶无色溶液分别是氯化钠和氢氧化钠溶液,下列鉴别方法中正确的是( )
| A、分别滴加酚酞试液看颜色变化 |
| B、分别加稀盐酸看现象 |
| C、取溶液蒸干,看有没有固体析出 |
| D、分别通二氧化碳后再加澄清石灰水,看有没有沉淀 |
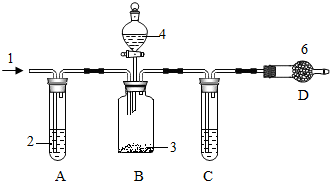
 某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应,也不溶于水的固体杂质)于烧杯中,加入9.8%的稀硫酸100g,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题:
某同学称取一定质量的铁粉样品(含有少量不与稀硫酸反应,也不溶于水的固体杂质)于烧杯中,加入9.8%的稀硫酸100g,恰好完全反应,生成气体的质量与反应时间的关系如图所示,试回答下列问题: