题目内容
纯碱中常含有少量的NaCl等杂质,利用如图的仪器装置测定纯碱中Na2CO3百分含量.
a.按如图所示组装实验仪器,并检查气密性
b.准确称量盛有碱石灰干燥剂管的质量(设为m1克)
c.准确称量一定量的纯碱(设为n克),并将其放进广口瓶内
d.从分液漏斗缓缓滴入稀H2SO4,至不再产生气体为止
e.缓缓通入空气数分钟,然后称量干燥管中的总质量(设为m2克)
图中:1.空气 2.某溶液 3.纯碱 4.稀H2SO4 5.浓H2SO4 6.碱石灰
根据上述实验,回答问题:
(1)上述实验操作d和e都要“缓缓”进行,理由是 ,如果这两步做太快,则会导致实验测定结果 (填偏大、偏小或不变).
(2)该实验进行至操作e时,要缓缓通入空气数分钟,通入空气作用是 .装置A中应装的液体2应选用 ;装置A作用是 ;如果撤去A,直接向B中缓缓通入空气,则会导致实验测定结果 .
(3)装置C的作用是 ,如果撤去C,则会导致测定结果 .
(4)根据此实验,计算纯碱中Na2CO3的百分含量的数学式: .

a.按如图所示组装实验仪器,并检查气密性
b.准确称量盛有碱石灰干燥剂管的质量(设为m1克)
c.准确称量一定量的纯碱(设为n克),并将其放进广口瓶内
d.从分液漏斗缓缓滴入稀H2SO4,至不再产生气体为止
e.缓缓通入空气数分钟,然后称量干燥管中的总质量(设为m2克)
图中:1.空气 2.某溶液 3.纯碱 4.稀H2SO4 5.浓H2SO4 6.碱石灰
根据上述实验,回答问题:
(1)上述实验操作d和e都要“缓缓”进行,理由是
(2)该实验进行至操作e时,要缓缓通入空气数分钟,通入空气作用是
(3)装置C的作用是
(4)根据此实验,计算纯碱中Na2CO3的百分含量的数学式:
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,盐的化学性质
专题:科学探究
分析:(1)上述实验操作d和e都要“缓缓”进行,能使二氧化碳缓缓通过碱石灰,从而被碱石灰完全吸收;
(2)该实验进行至操作e时,要缓缓通入空气数分钟,能使生成的二氧化碳全部被碱石灰吸收;
氢氧化钠溶液能够吸收二氧化碳;
(3)浓硫酸能够吸收水蒸气;
(4)根据提供的数据可以计算纯碱的质量分数.
(2)该实验进行至操作e时,要缓缓通入空气数分钟,能使生成的二氧化碳全部被碱石灰吸收;
氢氧化钠溶液能够吸收二氧化碳;
(3)浓硫酸能够吸收水蒸气;
(4)根据提供的数据可以计算纯碱的质量分数.
解答:解:(1)上述实验操作d和e都要“缓缓”进行,理由是使反应产生的二氧化碳能被碱石灰完全吸收;
如果这两步做太快,则会导致二氧化碳不能被碱石灰完全吸收,从而导致实验测定结果偏小.
故填:使反应产生的二氧化碳能被碱石灰完全吸收;偏小.
(2)该实验进行至操作e时,要缓缓通入空气数分钟,通入空气作用是使生成的二氧化碳全部被碱石灰吸收;
装置A中应装的液体2应选用氢氧化钠溶液;
装置A作用是除去空气中的二氧化碳;
如果撤去A,直接向B中缓缓通入空气,则会导致空气中的二氧化碳被碱石灰吸收,从而导致实验测定结果偏大.
故填:使生成的二氧化碳全部被碱石灰吸收;氢氧化钠溶液;除去空气中的二氧化碳;偏大.
(3)装置C的作用是吸收水蒸气,如果撤去C,则会导致水蒸气被碱石灰吸收,从而导致测定结果偏大.
故填:偏大.
(4)设碳酸钠的质量为x,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 44
x (m2-m1)g
=
,
x=
,
则纯碱中Na2CO3的百分含量的数学式为
%.
故填:
%.
如果这两步做太快,则会导致二氧化碳不能被碱石灰完全吸收,从而导致实验测定结果偏小.
故填:使反应产生的二氧化碳能被碱石灰完全吸收;偏小.
(2)该实验进行至操作e时,要缓缓通入空气数分钟,通入空气作用是使生成的二氧化碳全部被碱石灰吸收;
装置A中应装的液体2应选用氢氧化钠溶液;
装置A作用是除去空气中的二氧化碳;
如果撤去A,直接向B中缓缓通入空气,则会导致空气中的二氧化碳被碱石灰吸收,从而导致实验测定结果偏大.
故填:使生成的二氧化碳全部被碱石灰吸收;氢氧化钠溶液;除去空气中的二氧化碳;偏大.
(3)装置C的作用是吸收水蒸气,如果撤去C,则会导致水蒸气被碱石灰吸收,从而导致测定结果偏大.
故填:偏大.
(4)设碳酸钠的质量为x,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,
106 44
x (m2-m1)g
| 106 |
| x |
| 44 |
| (m2-m1)g |
x=
| 106×(m2-m1)g |
| 44 |
则纯碱中Na2CO3的百分含量的数学式为
| 10600×(m2-m1) |
| 44n |
故填:
| 10600×(m2-m1) |
| 44n |
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
用分子的相关知识解释下列现象,说法不正确的是( )
| A、热胀冷缩,说明分子的大小随温度的升降而改变 |
| B、经过食堂附近,闻到饭菜香味,说明分子在不断运动 |
| C、50mL水和50mL酒精混合后,总体积小于100mL,说明分子间有间隙 |
| D、燃烧的木条分别伸入集满氧气和二氧化碳的集气瓶中现象不同,说明分子不同化学性质不同 |
下列化学用语表示离子的是( )
①H2O2②Si③SO
④
.
①H2O2②Si③SO
2- 4 |
| +2 |
| Mg |
| A、①② | B、③④ | C、②④ | D、③ |
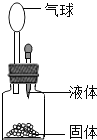 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是①生石灰和水;②石灰石和稀盐酸;③氢氧化钠固体和水;④硝酸铵和水( )
| A、①②③④ | B、①②③ |
| C、①②④ | D、②③④ |
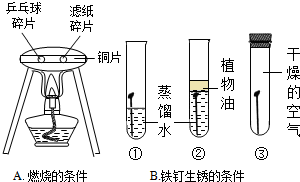 “对比实验”是化学学习中行之有效的思维方法.某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题.
“对比实验”是化学学习中行之有效的思维方法.某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题.