题目内容
20.下列除去杂质的方法中,错误的是( )| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 铁 | 铜 | 适量稀硫酸、过滤 |
| B | CaCl2溶液 | 稀盐酸 | 过量CaCO3、过滤 |
| C | ZnCl2溶液 | CuCl2 | 过量锌粉、过滤 |
| D | 氯化钠固体 | 泥沙 | 加水溶解、过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、稀盐酸能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、过量锌粉能与CuCl2反应生成氯化锌溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发结晶的方法进行分离除杂,故选项所采取的方法正确.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
6.下列除去杂质的方法中,合理的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | CO2 | CO | 点燃 |
| B | NaOH溶液 | Na2CO3溶液 | 加入适量稀盐酸 |
| C | 铜粉 | 铁粉 | 加入过量的稀硫酸,过滤 |
| D | CaO | CaCO3 | 加水,溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
8.FeSO4•7H2O是一种重要的补铁剂.某工业废渣主要成分是Fe2O3,还含有CaCO3和SiO2(SiO2既不溶于水也不溶于稀硫酸),实验室用此废渣制备FeSO4•7H2O的流程如下,请根据流程回答问题:

(1)加入的稀硫酸与粉末中的氧化铁反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,理论上为防止稀硫酸过量当溶液中不再产生气泡时即可停止向粉末中加入稀硫酸;
(2)经测定,滤渣中只含有CaSO4和SiO2,可推知实验室能(填”能”或者”不能”)用大理石粉末与稀硫酸反应制取二氧化碳;
(3)操作②所需要的玻璃仪器有烧杯、漏斗和玻璃棒,所缺少玻璃仪器的作用是引流;
(4)操作③中发生的反应除了置换反应外,还发生了其他反应,作出判断的依据是产物只有FeSO4一种或Fe2(SO4)3变成了FeSO4;
(5)已知硫酸亚铁的溶解度和析出晶体的组成如表:
根据上表,硫酸亚铁晶体(FeSO4•7H2O)冷却结晶温度最高不超过64;待结晶完毕后,滤出晶体,用少量硫酸亚铁饱和溶液洗涤2~3次,再用滤纸将晶体吸干.用硫酸亚铁饱和溶液洗涤的目的是:①洗去FeSO4晶体表面的杂质、②减少晶体的损耗.

(1)加入的稀硫酸与粉末中的氧化铁反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,理论上为防止稀硫酸过量当溶液中不再产生气泡时即可停止向粉末中加入稀硫酸;
(2)经测定,滤渣中只含有CaSO4和SiO2,可推知实验室能(填”能”或者”不能”)用大理石粉末与稀硫酸反应制取二氧化碳;
(3)操作②所需要的玻璃仪器有烧杯、漏斗和玻璃棒,所缺少玻璃仪器的作用是引流;
(4)操作③中发生的反应除了置换反应外,还发生了其他反应,作出判断的依据是产物只有FeSO4一种或Fe2(SO4)3变成了FeSO4;
(5)已知硫酸亚铁的溶解度和析出晶体的组成如表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
15.下列物质放入水中能形成无色透明溶液的是( )
| A. | 氯化钠 | B. | 汽油 | C. | 硫酸铜 | D. | 泥土 |
10.实验室用加热氯化铵和熟石灰固体混合物的方法制取氨气.根据装置图回答问题:

(1)实验室制取氨气的发生装置为C(填序号),该反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(2)氨气有刺激性气味,极易溶于水,收集氨气的最佳装置是F(填序号).
(3)小明认为制取氨气后的剩余固体中可能含有氢氧化钙,设计如下方案:取样品少量,加入适量的水溶解,滴加足量的碳酸钠溶液,有白色沉淀产生,说明含有氢氧化钙.小明的方案否(选填“是”、“否”)合理,理由是生成的氯化钙也能与碳酸钠反应生成白色沉淀.
(4)小红在实验时一直未能收集到氨气,分析原 因时,发现在装药品前忘记了某一操作,该操作为检查装置的气密性.改正后重新实验,仅收集到少量氨气,小红认为可能是熟石灰变质导致的,熟石灰变质的原因Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).为了进一步验证自己的猜想,设计如下方案:
请指出上述方案中错误的方案并说明理由方案1,氢氧化钙微溶于水.

(1)实验室制取氨气的发生装置为C(填序号),该反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(2)氨气有刺激性气味,极易溶于水,收集氨气的最佳装置是F(填序号).
(3)小明认为制取氨气后的剩余固体中可能含有氢氧化钙,设计如下方案:取样品少量,加入适量的水溶解,滴加足量的碳酸钠溶液,有白色沉淀产生,说明含有氢氧化钙.小明的方案否(选填“是”、“否”)合理,理由是生成的氯化钙也能与碳酸钠反应生成白色沉淀.
(4)小红在实验时一直未能收集到氨气,分析原 因时,发现在装药品前忘记了某一操作,该操作为检查装置的气密性.改正后重新实验,仅收集到少量氨气,小红认为可能是熟石灰变质导致的,熟石灰变质的原因Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).为了进一步验证自己的猜想,设计如下方案:
| 方案 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取少量样品于烧杯中,加水并搅拌 | 形成乳白色浊液 | 样品中只有CaCO3 |
| 2 | 取少量样品于烧杯中,加水并搅拌,静置,向上层清液中滴加酚酞 | 溶液变红 | 样品中一定含有Ca(OH)2 |
| 3 | 取少量样品于烧杯中,滴加足量的稀盐酸 | 产生气泡 | 样品中一定有CaCO3 |
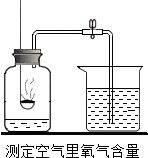 法国化学家拉瓦锡通过实验得出的结论是氧气约占空气总体积的$\frac{1}{5}$.某同学用如图装置进行验证,实验后发现气体减少的体积小于$\frac{1}{5}$,请你帮助这位同学找出两种可能造成这样结果的原因:
法国化学家拉瓦锡通过实验得出的结论是氧气约占空气总体积的$\frac{1}{5}$.某同学用如图装置进行验证,实验后发现气体减少的体积小于$\frac{1}{5}$,请你帮助这位同学找出两种可能造成这样结果的原因: