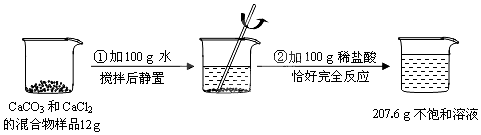
题目内容
20.水能灭火,是不是所有物质燃烧都可以用水灭火呢?小星查阅资料发现在金属活动性顺序表中靠前的金属钠在常温下可以和水反应生成一种能使酚酞溶液变红的物质和燃烧时火焰呈淡蓝色的气体单质,试写出该化学方程式2Na+2H2O═2NaOH+H2↑,该反应的基本反应类型是置换反应.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.
解答 解:金属钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O═2NaOH+H2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
故答案为:2Na+2H2O═2NaOH+H2↑;置换反应;
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
相关题目
11.工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:
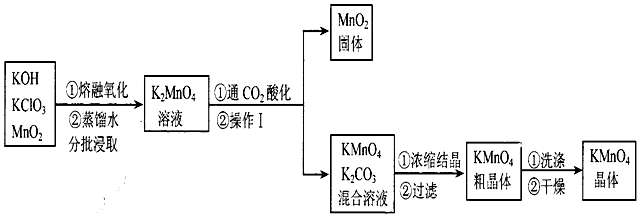
已知相关物质的溶解度(20℃)如下表:
(1)KMnO4中锰元素的化合价为+7.
(2)操作I的名称是过滤.“干燥”过程中温度不宜过高的原因是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MnO4+2CO2═2KMnO4+MnO2↓+2K2 CO3
若用稀H2SO4酸化,反应的化学方程式为:3K2 MnO4+2H2 SO4═2KMnO4+MnO2↓+2K2SO4+2H2O
工业上不采用稀H2SO4酸化的原因是相同条件下,硫酸钾和高锰酸钾溶解度都比较小,无法采用浓缩结晶的方法加以分离.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,同时还生成一种碱和一种单质气体.试写出其反应的化学方程式为:2K2MnO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑.与“通CO2酸化”相比,其优点是生成的氢氧化钾可以循环使用.

已知相关物质的溶解度(20℃)如下表:
| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
(2)操作I的名称是过滤.“干燥”过程中温度不宜过高的原因是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MnO4+2CO2═2KMnO4+MnO2↓+2K2 CO3
若用稀H2SO4酸化,反应的化学方程式为:3K2 MnO4+2H2 SO4═2KMnO4+MnO2↓+2K2SO4+2H2O
工业上不采用稀H2SO4酸化的原因是相同条件下,硫酸钾和高锰酸钾溶解度都比较小,无法采用浓缩结晶的方法加以分离.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,同时还生成一种碱和一种单质气体.试写出其反应的化学方程式为:2K2MnO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑.与“通CO2酸化”相比,其优点是生成的氢氧化钾可以循环使用.
15.下列鉴别物质所用的方法或试剂,错误的是( )
| A. | 氧气和氮气--观察颜色 | |
| B. | 酒和醋----闻气味 | |
| C. | 氢氧化钠和硝酸铵-加水,测量温度变化情况 | |
| D. | 氢氧化钠和盐酸--用紫色石蕊试液 |
12.电热水袋中的水加热后袋子膨胀,是因为袋内的水( )
| A. | 分子体积变大 | B. | 分子质量变大 | ||
| C. | 分子个数变多 | D. | 分子之间空隙变大 |
9.下列物质的俗称、化学式相一致的是( )
| A. | 苛性钠Na2CO3 | B. | 干冰H2O | C. | 生石灰Ca(OH)2 | D. | 水银Hg |
10.下列物质由离子直接构成的是( )
| A. | 水 | B. | 氯化钠 | C. | 金刚石 | D. | 二氧化碳 |