题目内容
9.下列物质中,含有氧分子的是( )| A. | H2O2 | B. | MnO2 | C. | CO2 | D. | O2 |
分析 物质中含有氧气的分子即是该物质中含有氧气,据此进行判断分析即可.
解答 解:
A、H2O2中含有氧元素,而无氧气分子,故不符合题意;
B、二氧化锰中含有氧元素,而无氧气分子,故不符合题意;
C、CO2中含有氧元素,而无氧气分子,故不符合题意;
D、氧气中含有氧分子,故符合题意.
故选D.
点评 解答本题的关键是要充分理解物质的组成,进而判断是否含有氧气的分子,只有这样才能对问题做出正确的判断.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
20.化学科学的发展离不开定量研究.下列有关定量实验的分析中,不正确的是( )
| A. | 木炭在氧气中燃烧时,氧气质量的多少会导致生成物不同 | |
| B. | 用量筒量取一定体积的液体时,若仰视刻度,则取得液体偏多 | |
| C. | 测定空气中氧气含量的实验中,红磷质量的多少不影响实验结果 | |
| D. | 用红磷燃烧探究质量守恒的实验中,红磷质量的多少不影响实验结果 |
17.下列可用于验证 Fe、Cu、Ag 三种金属的活动性顺序的一组药品是( )
| A. | Fe、Ag、CuSO4溶液 | B. | Cu、Ag、FeSO4 溶液 | ||
| C. | Fe、Cu、H2SO4 溶液 | D. | Ag、FeSO4 溶液、CuSO4 溶液 |
14.某同学学完第七章后,对“复分解反应发生的条件”进行了如下科学探究活动.
(1)提出问题:发生复分解反应应具备哪些条件?
(2)猜想与假设:
①酸、碱、盐的溶液混和后,溶液中自由移动的离子变少了,反应就发生了;
②酸、碱、盐的溶液混和后,肉眼能看到新物质的产生(例如,有沉淀或气体),反应才发生.
(3)进行实验并观察实验现象,请结合实验完成如表:
(4)解释与结论:
上述反应为什么能够发生?是因为在这些反应物中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如①中有Ba2++SO${\;}_{4}^{2-}$═BaSO4↓,②中有2H++CO${\;}_{3}^{2-}$═H2O+CO2↑,③中有H++OH-=H2O,④中有Ba2++CO32-→BaCO3↓,⑤中有NH4++OH-→NH3↑+H2O,从而使化学反应得以发生.经过分析,同学们得出的结论,猜想①正确.
(1)提出问题:发生复分解反应应具备哪些条件?
(2)猜想与假设:
①酸、碱、盐的溶液混和后,溶液中自由移动的离子变少了,反应就发生了;
②酸、碱、盐的溶液混和后,肉眼能看到新物质的产生(例如,有沉淀或气体),反应才发生.
(3)进行实验并观察实验现象,请结合实验完成如表:
| 实验步骤 | 实验现象 | 化学反应方程式 |
| 1酸钡溶液中滴加稀硫酸 | 有白色沉淀生成 | H2SO4+Ba(NO3)2═BaSO4↓+2HNO3 |
| ②稀硫酸溶液中滴加碳酸钾溶液 | 冒气泡 | H2SO4+K2CO3═K2SO4+CO2↑+H2O |
| ③稀盐酸溶液中先加2滴酚酞试液,再滴加氢氧化钠溶液 | 溶液由无色变浅红色,并不腿色 | HCl+NaOH=NaCl+H2O |
| ④硝酸钡溶液中滴加碳酸钾溶液 | 有白色沉淀生成 | Ba(NO3)2+K2CO3=BaCO3↓+2KNO3 |
| ⑤氯化铵溶液中滴加浓氢氧化钠溶液后加热,并用湿润的红色石蕊试纸检验生成的气体 | 有无色、刺激性气味的气体生成,该气体能使红色石蕊试纸变蓝 | NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+NH3↑+H2O |
上述反应为什么能够发生?是因为在这些反应物中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如①中有Ba2++SO${\;}_{4}^{2-}$═BaSO4↓,②中有2H++CO${\;}_{3}^{2-}$═H2O+CO2↑,③中有H++OH-=H2O,④中有Ba2++CO32-→BaCO3↓,⑤中有NH4++OH-→NH3↑+H2O,从而使化学反应得以发生.经过分析,同学们得出的结论,猜想①正确.
1.下列图象关系合理的是( )
| A. |  向CaCl2和HCl混合溶液中加入Na2CO3溶液 | |
| B. | 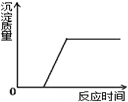 向CuSO4和H2SO4混合溶液中加入NaOH 溶液 | |
| C. |  分别向等质量的Fe和Mg中加入等浓度的稀硫酸 | |
| D. | 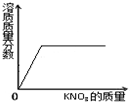 向接近饱和的KNO3溶液中加KNO3固体 |
18.元素周期表中氧元素的有关信息如右图所示,从图中不能直接获得的信息是( )
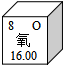

| A. | 氧元素属于非金属元素 | B. | 氧元素的原子序数为8 | ||
| C. | 氧元素的相对原子质量为16.00 | D. | 氧元素有O2和O3两种单质 |

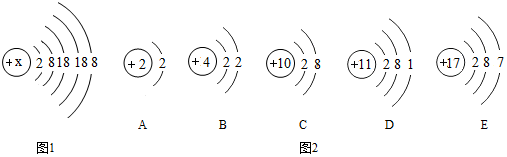
 小明同学对探究分子性质的实验(图1)进行了改进.如图2所示,试管丁、戊中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的小药瓶固定在橡皮塞上,试管丁中小药瓶上的瓶塞已塞紧,试管戊中的小药瓶上无瓶塞.关于图1、图2中的实验有以下说法:
小明同学对探究分子性质的实验(图1)进行了改进.如图2所示,试管丁、戊中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的小药瓶固定在橡皮塞上,试管丁中小药瓶上的瓶塞已塞紧,试管戊中的小药瓶上无瓶塞.关于图1、图2中的实验有以下说法: