题目内容
12.围绕一瓶长久暴露在空气中的NaOH固体是否变质生成Na2CO3的问题,同学们展开探究活动.查阅资料:Na2CO3溶液的pH>7.某同学欲证明变质固体中尚存NaOH,请你帮助他完成以下探究方案.| 探究步骤 | 实验目的 |
| ①取少量固体溶于水,滴加足量的BaCl2溶液 | 目的是将碳酸钠完全除掉,以防对氢氧化钠的检验产生干扰 |
| ②向①步骤所得溶液中滴加酚酞试液 | 根据颜色变化情况判断是否存在NaOH |
分析 ①氯化钡能与碳酸钠反应生成氯化钠和碳酸钡沉淀;
②根据碱的性质来分析.
解答 解:①欲检验碳酸钠中是否含有氢氧化钠,加入足量的BaCl2溶液是为了将碳酸钠完全反应掉,而转化为碳酸钡沉淀和氯化钠(中性),碳酸钠溶液显碱性,以防对氢氧化钠的检验产生干扰;故填:将碳酸钠完全除掉,以防对氢氧化钠的检验产生干扰;
②氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,故填:酚酞.
点评 本题考查了氢氧化钠变质情况的检验和证明,要注意氢氧化钠和碳酸钠二者碱性的干扰,因此要证明氢氧化钠的存在,须先加入中性盐溶液将碳酸钠转化成沉淀除去

练习册系列答案
相关题目
17.地震中自来水厂严重受损,供水网受损,水源收到污染,给居民饮用水造成困难.下列说法正确的是( )
| A. | 自来水厂生产的自来水是纯净物 | |
| B. | 净化水的常用方法有沉淀、过滤、吸附、蒸馏等 | |
| C. | 在自来水的生产过程中,加入活性炭是利用它的化学性质来净化 | |
| D. | 自来水厂可用硫酸铜给饮用水消毒 |
17.下列有关溶液中的认识正确的是( )
| A. | KNO3的溶解度为31.6g | B. | 研究溶液性质时,溶质宜为一种 | ||
| C. | 常温下,饱和石灰水无法溶解溶质 | D. | 温度是影响气体溶解量的主要原因 |
4.为挖掘弘扬临海美食,丰富群众生活,我市在2012中国临海古城文化节活动期间(11月21日至11月25日)将在临海市体育中心西广场(张洋路边)举办临海特色风味美食节.白水洋豆腐是临海美食节上的一道名菜.在豆腐加工时需加入凝固剂,凝固剂的化学成分是什么?通过查资料获悉:凝固剂中可能含有Na2SO4、Ca(OH)2、MgCl2、NaCl等,为验证其成分,小白,小水和小洋进行了如下实验:
(1)根据以上现象,凝固剂溶液中肯定没有Ca(OH)2(或氢氧化钙);
(2)写出实验2中发生的化学反应方程式Ba(N03)2+Na2S04=BaS04↓+2NaN03;
(3)写出实验3中出现的白色沉淀物质的化学式AgCl.
| 实验 | 实验操作 | 实验现象 |
| 1 | 取少量凝固剂溶液于试管中,加入几滴无色酚酞试液 | 仍为无色溶液 |
| 2 | 再取少量凝固剂溶液于试管中,加入适量的Ba(NO3)2溶液和过量稀HNO3 | 有白色沉淀 |
| 3 | 取实验2中的适量滤液于试管中,加入适量的AgNO3溶液和稀HNO3 | 有白色沉淀 |
(2)写出实验2中发生的化学反应方程式Ba(N03)2+Na2S04=BaS04↓+2NaN03;
(3)写出实验3中出现的白色沉淀物质的化学式AgCl.
1.下列是我市2015年基本实验操作考试中的部分考生的操作,其中没有错误的是( )
| A. | 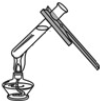 加热液体 | B. |  倾倒液体 | C. |  量取液体 | D. | 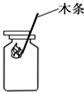 氧气验满 |
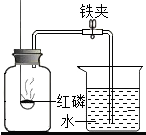 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛有红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛有红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题: