题目内容
16.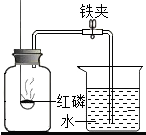 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛有红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛有红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:(1)该反应的符号表达式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.反应现象:剧烈地燃烧,产生大量的白烟.
(2)小涵用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是:①装置气密性不好;②红磷量不足;③没有冷却到室温就读数.
(3)小盈也设计了一个实验方案,装置和操作同上,只不过用木炭代替红磷.当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶?为什么?不会;碳与氧气反应生成了二氧化碳气体,没有产生压强差.
分析 (1)红磷在空气中能够剧烈地燃烧,放出大量的热,产生大量的白烟;
(2)红磷不足、装置漏气、点燃后没有迅速伸入集气瓶并塞紧橡皮塞、没有冷却到室温就打开弹簧夹等都可以使测定的结果不准确;
(3)用木炭代替了红磷,水不会进入集气瓶,因为碳与氧气反应生成了二氧化碳气体,内外没有产生压强差.
解答 解:(1)红磷在空气中能够剧烈地燃烧,产生大量的白烟;红磷燃烧是红磷与空气中的氧气反应,生成五氧化二磷,故反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)保证本实验成功的关键是:装置气密性要好;红磷要足量;要冷却到室温再读数.故答案为:装置气密性不好;红磷量不足;或没有冷却到室温就读数;
(3)用木炭代替了红磷,水不会进入集气瓶,因为碳与氧气反应生成了二氧化碳气体,内外没有产生压强差.故答案为:不会;碳与氧气反应生成了二氧化碳气体,没有产生压强差.
答案:
(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;剧烈地燃烧,产生大量的白烟;
(2)装置气密性不好;红磷量不足;没有冷却到室温就读数;
(3)不会;碳与氧气反应生成了二氧化碳气体,没有产生压强差.
点评 本考点考查的是空气中氧气含量的探究实验,根据实验操作图,回忆实验中现象,由实验中的注意事项,对实验结果进行评价,从而理解该实验的探究目的.对实验结果进行评价,是近几年中考的重点之一,要好好把握.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
4.为完全中和某NaOH溶液,需消耗一定量的盐酸,如改用与盐酸等质量、且等质量分数的硫酸,则反应后溶液的pH将( )
| A. | 大于7 | B. | 小于7 | C. | 等于7 | D. | 等于0 |
1.下列四种变化中,与其它三种变化有本质区别的一种是( )
| A. | 铁放在潮湿的空气中质量增加 | |
| B. | 氢氧化钠固体放在空气中质量增加 | |
| C. | 浓盐酸敞口放在置在空气中质量减轻 | |
| D. | 硫酸铜晶体受热,颜色改变 |
8.下列有关实验现象的描述正确的是( )
| A. | 红磷燃烧产生白雾 | |
| B. | 铁和稀硫酸反应溶液为棕黄色 | |
| C. | NaCl溶液进行焰色反应时火焰呈紫色 | |
| D. | 将二氧化碳通入水中无明显现象 |
12.围绕一瓶长久暴露在空气中的NaOH固体是否变质生成Na2CO3的问题,同学们展开探究活动.查阅资料:Na2CO3溶液的pH>7.某同学欲证明变质固体中尚存NaOH,请你帮助他完成以下探究方案.
| 探究步骤 | 实验目的 |
| ①取少量固体溶于水,滴加足量的BaCl2溶液 | 目的是将碳酸钠完全除掉,以防对氢氧化钠的检验产生干扰 |
| ②向①步骤所得溶液中滴加酚酞试液 | 根据颜色变化情况判断是否存在NaOH |
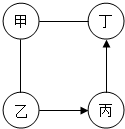 如图中甲、乙、丙、丁是初中化学中常见的物质,均由两种或三种元素组成,其中甲是胃液中帮助消化的成分,乙俗称消石灰.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.
如图中甲、乙、丙、丁是初中化学中常见的物质,均由两种或三种元素组成,其中甲是胃液中帮助消化的成分,乙俗称消石灰.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去. 如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题.
如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题.