题目内容
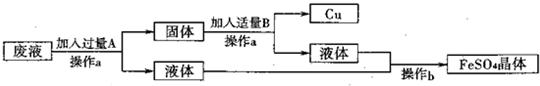
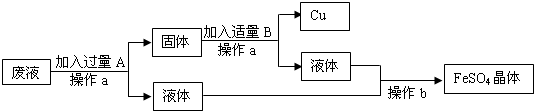
17、某工厂欲从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
(提示:硫酸亚铁溶液的溶解度受温度变化影响不大)
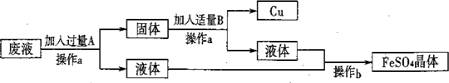
(1)A是
B是
(2)操作a的名称是
(3)从液体中获取硫酸亚铁晶体的操作方法b是
(提示:硫酸亚铁溶液的溶解度受温度变化影响不大)

(1)A是
铁(或Fe)
,加入过量A的目的是将废液中的CuSO4完全反应掉
;B是
稀硫酸(或H2SO4)
,利用其除去铜中杂质,有关反应的化学方程式Fe+H2SO4=FeSO4+H2↑
.(2)操作a的名称是
过滤
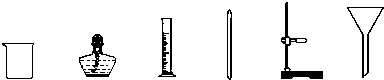
,进行该操作所需的玻璃仪器玻璃棒
有烧杯、漏斗
(请从下图中选择合适仪器,并用仪器名称填写).
(3)从液体中获取硫酸亚铁晶体的操作方法b是
蒸发结晶
.分析:在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,故要回收铜得到硫酸亚铁,可以加入铁.
解答:解:(1)铁的金属性比铜强,可置换出硫酸铜中的铜,为使硫酸铜全部反应必须加过量的铁;铁溶解玉酸所以加稀硫酸可除去铜中的铁;故答案为:铁、将废液中的CuSO4完全反应掉、稀硫酸(或H2SO4)、Fe+H2SO4═FeSO4+H2↑
(2)经过操作a能得到固体和液体,故a操作为过滤,过滤中需玻璃棒进行引流,用漏斗制过滤器,所以本题答案为:过滤、玻璃棒、漏斗;
(3)硫酸亚铁溶液中得到晶体硫酸亚铁,可采用蒸发的方法,所以本题答案为:蒸发结晶
(2)经过操作a能得到固体和液体,故a操作为过滤,过滤中需玻璃棒进行引流,用漏斗制过滤器,所以本题答案为:过滤、玻璃棒、漏斗;
(3)硫酸亚铁溶液中得到晶体硫酸亚铁,可采用蒸发的方法,所以本题答案为:蒸发结晶
点评:本题考查了铜的回收,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目