题目内容
3.如图是粗盐提纯实验的部分操作,请回答相关问题.
(1)如图所示操作中,有错误的是C(填字母).
(2)粗盐提纯的正确操作顺序为DACB(填字母).
(3)操作A、B、C中,玻璃棒的作用分别是搅拌,加快物质的溶解、使受热均匀,防止液滴飞溅,引流.
(4)步骤D中称取10.0g粗盐,将该粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,称得剩余粗盐为2.0g,最终得到NaCl晶体3.2g,该实验精盐的产率是40%.
(5)、过滤,过滤食盐水,滤液仍浑浊,可更换滤纸,重新过滤;
(6)若制得的精盐的产率偏高,则可能的原因是AC(填字母).
A、过滤时滤纸有破损 B、蒸发时有固体溅出 C、最终所得精盐比较潮湿.
分析 (1)过滤要用玻璃棒进行引流,可以据此解答该题;
(2)粗盐提纯的正确的顺序是溶解、过滤、蒸发、结晶,可以据此结合题给的选项进行解答;
(3)根据不同操作中玻璃棒的作用解答该题;
(4)根据产率的计算方法进行计算即可;
(5)滤液中还含有难溶性固体可重新过滤一次;
(6)根据产率的计算公式结合操作过程中可能出现的问题进行解答.
解答 解:(1)过滤要用玻璃棒进行引流,分析图中所示可以知道C中的过滤操作有错误,故选C;
(2)粗盐提纯的正确的顺序是溶解、过滤、蒸发、结晶,所以正确的顺序为:DACB;
(3)操作A是溶解,此过程中玻璃棒的作用是搅拌,加快物质的溶解;操作B为蒸发,该过程中玻璃棒的作用是搅拌,以使溶液受热均匀;操作C是过滤,此过程中玻璃棒的作用是引流;
(4)根据题意可以知道溶解的粗盐的质量为:10.0g-2.0g=8.0g,而最终得到精盐的质量为3.2g,
所以精盐的产率为:$\frac{3.2g}{8g}$×100%=40%;
(5)若滤液仍然浑浊,可进行更换滤纸,重新过滤;
(6)若制得的精盐的产率偏高,则说明得到精盐的质量偏大,分析所给的选项可以知道:
A、过滤时滤纸破损,则会使部分杂质得不到过滤,而使蒸发的得到的精盐的质量偏大,故可能导致产率偏高,故A正确;
B、蒸发时有固体飞溅出来,则会使得到的精盐的质量偏小,而使精盐的产率偏低,故B错误;
C、最终所得精盐比较潮湿,即称得的精盐质量偏大,所以会导致产率偏高,故C正确.
故选AC.
故答案为:(1)C;(2)DACB;(3)搅拌,加快物质的溶解;使受热均匀,防止液滴飞溅;引流;(4)40%;(5)更换滤纸,重新过滤;(6)AC.
点评 要想解答好这类题目,首先,要理解和熟记氯化钠与粗盐提纯等相关知识.然后,根据所给的实验、问题情景等,结合所学的相关知识和技能,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

 口算能手系列答案
口算能手系列答案| A. | 质子数不同 | B. | 中子数不同 | ||
| C. | 相对原子质量不同 | D. | 电子数不同 |
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |

(2)曲线上M点的含义是t1℃时,KNO3和K2CO3的溶解度相等;.
(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的有ACE.(填字母)
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液X
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
E.将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变.
| A. | 18 g | B. | 4.5 g | C. | 2.25 g | D. | 36 g |
| A. | 分子和原子都在不断运动 | B. | 化学变化中原子不能再分 | ||
| C. | 原子核由质子和电子构成 | D. | 原子的质量主要集中在原子核上 |
| A. | 茶氨酸属于混合物,锌、硒指单质 | |
| B. | 一个茶氨酸分子中含3个氧原子 | |
| C. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| D. | 茶树不宜在碱性土壤中生长 |
 向实验室制取二氧化碳后的剩余溶液中,逐滴加入碳酸钠溶液至过量,该实验中溶液pH变化曲线如图所示.(提示:氯化钙溶液呈中性)
向实验室制取二氧化碳后的剩余溶液中,逐滴加入碳酸钠溶液至过量,该实验中溶液pH变化曲线如图所示.(提示:氯化钙溶液呈中性)
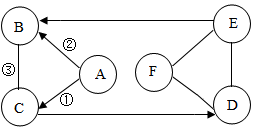 A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)
A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)