题目内容
6.下列各组物质按单质、氧化物、混合物的顺序排列的是( )| A. | 钢、氧化镁、空气 | B. | 稀有气体、水、果汁 | ||
| C. | 氮气、氧气、牛奶 | D. | 金刚石、冰水、矿物质水 |
分析 纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物;
氧化物是由氧元素和另外一种元素组成的化合物.
解答 解:A、钢的主要成分是铁,还含有碳等物质,属于混合物;氧化镁是由镁元素和氧元素组成的化合物,属于氧化物;空气中含有氮气、氧气等物质,属于混合物;
B、稀有气体中含有氦气、氖气等物质,属于混合物;水是由氢元素和氧元素组成的化合物,属于氧化物;果汁中含有水和一些溶于水的物质,属于混合物;
C、氮气是由氮元素组成的纯净物,属于单质;氧气是由氧元素组成的纯净物,属于单质;牛奶中含有水、蛋白质等物质,属于混合物;
D、金刚石是由碳元素组成的纯净物,属于单质;冰是水的固体,冰水混合物中含有一种物质--水,水是由氢元素和氧元素组成的化合物,属于氧化物;矿物质水中含有水和溶于水的矿物质,属于混合物.
故选:D.
点评 判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物、氧化物时,既要判断元素组成,又要判断物质组成.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
16.室温时,将1g蔗糖放入100g水中,充分溶解,形成溶液.蔗糖分子发生变化的是( )
| A. | 大小 | B. | 个数 | C. | 种类 | D. | 间隔 |
17.鉴别二氧化碳、氧气、空气三种气体,可选用的最佳方法是( )
| A. | 将气体分别通入水中 | B. | 将燃着的木条分别伸入气体中 | ||
| C. | 将带火星的木条分别伸入气体中 | D. | 将气体分别通入澄清石灰水中 |
14.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想三,H2SO4和NaOH在溶液中不能共存.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如硫酸和氢氧化钠反应中,实际参加反应的离子是H+和OH一,而SO42-、Na+则是“旁观者”,并没有参加反应.请你分析澄清石灰水和碳酸钠溶液反应中,参加反应的离子是Ca2+和CO32-.
【实验推广2】中和反应是没有现象的,如果要鉴别三瓶液体:稀硫酸,澄清石灰水,食盐水.提供试剂有:(A)酚酞,(B)纯碱溶液,只用一种试剂就可以将这三瓶液体区分出来,则选用试剂可以是B(从提供的试剂中选用)
Ⅱ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:

计算反应后溶液中Na2SO4的质量是多少?(请列出计算过程)
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想三,H2SO4和NaOH在溶液中不能共存.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2 溶液 |
| 实验操作 | 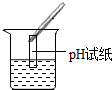 | 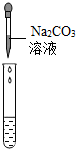 | 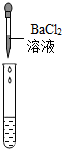 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【实验推广1】你想过复分解反应为什么能够发生吗?这是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如硫酸和氢氧化钠反应中,实际参加反应的离子是H+和OH一,而SO42-、Na+则是“旁观者”,并没有参加反应.请你分析澄清石灰水和碳酸钠溶液反应中,参加反应的离子是Ca2+和CO32-.
【实验推广2】中和反应是没有现象的,如果要鉴别三瓶液体:稀硫酸,澄清石灰水,食盐水.提供试剂有:(A)酚酞,(B)纯碱溶液,只用一种试剂就可以将这三瓶液体区分出来,则选用试剂可以是B(从提供的试剂中选用)
Ⅱ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:

计算反应后溶液中Na2SO4的质量是多少?(请列出计算过程)
11.为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )
| 选项 | 物质(杂质) | 操作方法 |
| A | Cu(Fe) | 加足量稀硫酸,充分反应后过滤 |
| B | CO(O2) | 缓慢通过灼热铜网 |
| C | KNO3溶液(少量NaCl) | 冷却热饱和溶液 |
| D | FeSO4溶液(CuSO4) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
15.下列物质在空气中长时间敞口放置,质量减轻的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 生石灰 |
16.下列实验设计不合理的是 ( )
| A. | 除去氯化钠中混有的泥沙:溶解→过滤→蒸发 | |
| B. | 除去氯化亚铁溶液中混有的氯化铜:加过量的铁粉→过滤 | |
| C. | 除去碳酸钙中混有的氯化钙:加水→过滤→洗涤→干燥 | |
| D. | 除去氢氧化钠固体中混有的碳酸钠:加水→加适量稀盐酸→过滤→蒸发 |