题目内容
18.小莉用6.5g锌与154.7g稀硫酸制取氢气恰好完全反应,求反应后溶液中溶质质量分数.(Zn+H2SO4═ZnSO4+H2↑)分析 锌和稀硫酸反应生成了硫酸锌和氢气,稀硫酸是混合物,不能将其质量带入进行计算,故根据锌的质量可以计算出生成的氢气的质量和硫酸锌的质量,然后结合溶液溶质的质量分数计算公式完成解答即可.
解答 解:设硫酸锌质量为x,氢气质量为y
Zn+H2SO4═ZnSO4+H2↑
65 161 2
6.5g x y
$\frac{65}{6.5g}=\frac{161}{x}=\frac{2}{y}$
X=16.1g
Y=0.2g
反应后溶液中溶质质量分数=$\frac{16.1g}{6.5g+154.7g-0.2g}×100%$=10%
答:反应后溶液中溶质质量分数10%.
点评 本题主要考查了根据化学方程式的计算,解题的关键是根据质量守恒定律求出反应后生成的溶液的质量.

练习册系列答案
相关题目
8.区分下列各组物质所用的两种方法都正确的是( )
| 选项 | 需要区分的物质 | 方法一 | 方法二 |
| A | 黄金和黄铜 | 观察颜色 | 取样,分别滴加稀盐酸 |
| B | 硝酸钾和硝酸铵 | 分别溶于水,测温度 | 取样,加熟石灰研磨 |
| C | 生铁和钢 | 取样,分别加入硫酸铜溶液 | 分别用磁铁吸引 |
| D | 白酒和白醋 | 闻气味 | 取样,滴加酚酞 |
| A. | A | B. | B | C. | C | D. | D |
6.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
| A. | 钢、氧化镁、空气 | B. | 稀有气体、水、果汁 | ||
| C. | 氮气、氧气、牛奶 | D. | 金刚石、冰水、矿物质水 |
3.下列实验操作正确的是( )
| A. | 浓硫酸不小心沾到皮肤上,先用干布拭去,再立刻用稀NaOH溶液冲洗 | |
| B. | 称量氢氧化钠固体时,必须将所称药品放在托盘天平左盘上的洁净的纸上 | |
| C. | 为了测定某溶液的pH值,将干燥的pH试纸浸入待测溶液片刻后取出,再与标准比色卡进行对比 | |
| D. | 金属钠不慎燃烧不能用水扑灭,应立即用沙子覆盖 |
10.下列物质中,属于混合物的是( )
| A. | 矿泉水 | B. | 水银 | C. | 干冰 | D. | 液氧 |
7.苯的化学式为C6H6,下列有关苯的说法正确的是( )
| A. | 苯中的C、H元素的质量比为12:1 | |
| B. | 苯分子是由6个碳元素和6个氢元素组成 | |
| C. | 苯的相对分子质量为13 | |
| D. | 苯分子由6个碳原子和6个氢原子构成 |
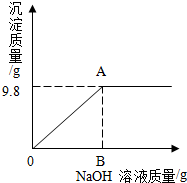 有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.
有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.