题目内容
7.某纯碱样品中含有少量氢氧化钠,小明取该纯碱样品11g,全部溶解在100g水中,再加入氢氧化钙溶液141g,恰好完全反应.过滤干燥后,称得沉淀质量为10g.请计算:(1)纯碱样品中碳酸钠的质量分数;
(2)反应后所得滤液的溶质质量分数.
分析 (1)根据氯化钠、碳酸钠的性质,氯化钠不能与加入的氢氧化钙发生反应,碳酸钠与氢氧化钙生成碳酸钙沉淀和氢氧化钠,根据生成沉淀碳酸钙的质量可计算样品中所含碳酸钠的质量;
(2)根据题中的数据求出氢氧化钠的质量和反应后溶液的质量,可以求出反应后所得滤液的溶质质量分数.
解答 解:(1)设恰好完全反应时参加反应的碳酸钠的质量为x,生成氢氧化钠的质量为y,
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100 80
x 10g y
$\frac{106}{x}$=$\frac{100}{10g}$=$\frac{80}{y}$
x=10.6g
y=8g
所以纯碱样品中碳酸钠的质量分数为:$\frac{10.6g}{11g}$×100%=96.4%;
纯碱样品中碳酸钠的质量分数为:$\frac{11g-10.6g+8g}{11g+100g+141g-10g}$×100%=3.5%.
故答案为:(1)96.4%;
(2)3.5%.
点评 根据化学方程式可以表示反应中各物质的质量关系,由其中任意一种物质的质量可计算反应中其它物质的质量.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 山林发生火灾时砍掉或清理掉大火前面的树枝等可燃物 | |
| B. | 酒精灯不慎翻倒失火时用水冲灭 | |
| C. | 炒菜时油锅中的油失火应立即盖上锅盖,关掉灶具 | |
| D. | 图书档案失火时选用泡沫灭火器灭火 |
2. 2009年3月1日16时13分,我国首颗探月卫星“嫦娥一号”在完成任务以后实行“受控撞月”,探测月壤是“嫦娥一号”的主要任务之一,因为月壤中蕴藏着丰富的氦-3,氦-3是一种安全高效而又清洁无污染的重要燃料,应用前景广阔.下列关于“氦-3”原子的说法正确的是( )
2009年3月1日16时13分,我国首颗探月卫星“嫦娥一号”在完成任务以后实行“受控撞月”,探测月壤是“嫦娥一号”的主要任务之一,因为月壤中蕴藏着丰富的氦-3,氦-3是一种安全高效而又清洁无污染的重要燃料,应用前景广阔.下列关于“氦-3”原子的说法正确的是( )
 2009年3月1日16时13分,我国首颗探月卫星“嫦娥一号”在完成任务以后实行“受控撞月”,探测月壤是“嫦娥一号”的主要任务之一,因为月壤中蕴藏着丰富的氦-3,氦-3是一种安全高效而又清洁无污染的重要燃料,应用前景广阔.下列关于“氦-3”原子的说法正确的是( )
2009年3月1日16时13分,我国首颗探月卫星“嫦娥一号”在完成任务以后实行“受控撞月”,探测月壤是“嫦娥一号”的主要任务之一,因为月壤中蕴藏着丰富的氦-3,氦-3是一种安全高效而又清洁无污染的重要燃料,应用前景广阔.下列关于“氦-3”原子的说法正确的是( )| A. | 与“氦-4”的中子数不同 | B. | 核电荷数与核外电子数可能不等 | ||
| C. | 质子数与核电荷数相等 | D. | 质子数与中子数相等 |
16.氯化钠是工业生产和生活的一种重要原料,也是厨房里常用的调味品“食盐”.下表是20℃时,氯化钠溶解于水的实验数据,请你分析并回答下列问题:
(1)计算第④次实验得到的氯化钠溶液的溶质质量分数.(精确到0.1%)
(2)n=136.
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是②③(填实验序号)
| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
| ① | 100 | 20 | 120 |
| ② | 100 | 30 | 130 |
| ③ | 100 | 40 | n |
| ④ | 100 | 50 | 136 |
(2)n=136.
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是②③(填实验序号)
 如图以稀硫酸例的反应关系体现了酸的化学性质,其中的X与图中所给物质的类别不同.结合此图回答下列问题:
如图以稀硫酸例的反应关系体现了酸的化学性质,其中的X与图中所给物质的类别不同.结合此图回答下列问题: “水循环”和“碳循环”是自然界存在的两大重要循环.结合你所学到的化学知识回答下面有关问题.
“水循环”和“碳循环”是自然界存在的两大重要循环.结合你所学到的化学知识回答下面有关问题.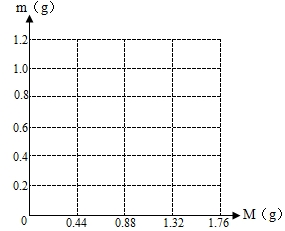 小翔做CO2的鉴定实验时发现一个新问题:二氧化碳通入澄清的石灰水后,澄清的石灰水会变浑浊,但为什么继续通二氧化碳后又变澄清了?查资料,原来碳酸钙和二氧化碳、水又反应生成了可溶性的碳酸氢钙.现将KCl和Ca(OH)2混合物1.85g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO20.44g.
小翔做CO2的鉴定实验时发现一个新问题:二氧化碳通入澄清的石灰水后,澄清的石灰水会变浑浊,但为什么继续通二氧化碳后又变澄清了?查资料,原来碳酸钙和二氧化碳、水又反应生成了可溶性的碳酸氢钙.现将KCl和Ca(OH)2混合物1.85g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO20.44g.