题目内容
19. 小翔做CO2的鉴定实验时发现一个新问题:二氧化碳通入澄清的石灰水后,澄清的石灰水会变浑浊,但为什么继续通二氧化碳后又变澄清了?查资料,原来碳酸钙和二氧化碳、水又反应生成了可溶性的碳酸氢钙.现将KCl和Ca(OH)2混合物1.85g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO20.44g.
小翔做CO2的鉴定实验时发现一个新问题:二氧化碳通入澄清的石灰水后,澄清的石灰水会变浑浊,但为什么继续通二氧化碳后又变澄清了?查资料,原来碳酸钙和二氧化碳、水又反应生成了可溶性的碳酸氢钙.现将KCl和Ca(OH)2混合物1.85g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO20.44g.(1)求原混合物中Ca(OH)2的质量分数;
(2)根据题意,在图示坐标系上,画出生成沉淀的质量m(g)与通入CO2的质量M(g)的关系曲线.
分析 (1)根据二氧化碳的质量计算出消耗的氢氧化钙的质量;
(2)根据取极值法求出最大值和最小值,进行连线.
解答 解:(1)设与0.44g二氧化碳反应消耗氢氧化钙的质量为X,生成沉淀质量为Y,则:
CO2+Ca(OH)2═CaCO3↓+H2O
44 74 100
0.44g X Y
$\frac{44}{0.44g}$=$\frac{74}{X}$=$\frac{100}{Y}$
X=0.74g
Y=1g
所以氢氧化钙的质量分数为:$\frac{0.74g}{1.85g}$×100%=40%;
(2)CO2+Ca(OH)2═CaCO3↓+H2O
44 100
M m
$\frac{44}{M}$=$\frac{100}{m}$
m=$\frac{100M}{44}$,M的取值为0≤M<0.44;
CaCO3+H2O+CO2═Ca(HCO3)2
100 44
m M
$\frac{100}{m}$=$\frac{44}{M}$
m=$\frac{100M}{44}$,
但是这是二氧化碳多于0.44g后消耗的碳酸钙的质量关系,所以还剩碳酸钙的质量等于生成碳酸钙最大值1减去消耗的碳酸钙的质量即:m=1-$\frac{100(M-0.44)}{44}$,
M取值范围:0.44≤M≤0.88;
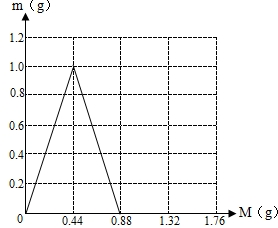
(3)生成碳酸钙最大值是1,再通入二氧化碳碳酸钙就会减少,当通到0.88g二氧化碳碳酸钙正好被消耗完.把0点、1g、0.88三个点连接起来即可.
故答案为:(1)40%;
(2)
点评 解答本题容易出错的地方是碳酸钙与二氧化碳、水反应生成碳酸氢钙,使沉淀减少.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
9.如图是A、B、C三种固体物质的溶解度曲线,下列说法中不正确的是( )
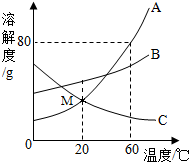

| A. | 60℃时A物质的溶解度最大 | |
| B. | 升高温度可使C物质的不饱和溶液转化为饱和溶液 | |
| C. | M点表示的是20℃时AC的溶解度相等 | |
| D. | 当B中含有少量A时,可用蒸发溶剂的方法提纯分离B | |
| E. | 60℃ABC的饱和溶液降温至20℃,溶液中溶质的质量分数由大到小的顺序是B>A=C |
10.下表中给出部分信息,请根据已有信息进行填空:
| 物质名称 | 化学式 | 物质种类 |
| C | ||
| 二氧化碳 | ||
| CH4 | ||
| 乙醇 | ||
| Na2CO3 | ||
| 葡萄糖 | ||
| Ca(OH)2 | ||
| 硫酸 |
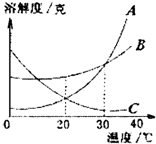 如图所示为A、B、C三种同体物质的溶解度曲线.
如图所示为A、B、C三种同体物质的溶解度曲线. 表示氢原子,
表示氢原子, 表示氧原子),其中能保持水的化学性质的是( )
表示氧原子),其中能保持水的化学性质的是( )