题目内容
4.小明同学用加热氯酸钾和二氧化锰的混合物制取氧气,加热一段时间后,制得所需气体,停止加热.甲乙丙三位同学对试管中剩余固体成分产生了兴趣,作出了以下三种猜想:甲:氯化钾、二氧化锰
乙:氯酸钾、氯化钾、二氧化锰
丙:氯酸钾、氯化钾
以上猜想中,丙的猜想是错误的,理由一是反应后的物质中没有二氧化锰;理由二是二氧化锰是该反应的催化剂,催化剂在反应前后,质量不变(注:该问可结合实验过程中的真实现象回答).
甲乙同学,为了验证自己的猜想,分别做了如下实验:
甲同学的实验报告如下:
| 实验方法 | 现象 | 结论 |
| 取样,溶于水后过滤 | 得到无色溶液和黑色固体 | 是氯化钾和二氧化锰 |
假如乙同学的猜想正确,请你帮助他完成下列实验报告:
| 实验方法 | 现象 | 结论和反应的符号表达式 |
| 猜想正确 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
分析 根据催化剂在反应前后质量和化学性质都不会改变进行分析;
根据氯酸钾、氯化钾易溶于水进行分析;
根据氯酸钾在二氧化锰的催化作用下会生成氧气,氧气有助燃性进行分析.
解答 解:催化剂在反应前后质量和化学性质都不会改变,所以以上猜想中,丙的猜想是错误的,理由一是反应后的物质中没有二氧化锰,理由二是二氧化锰是该反应的催化剂,催化剂在反应前后,质量不变;
氯酸钾、氯化钾易溶于,所以甲同学的实验不合理,理由是:氯酸钾也易溶于水;
氯酸钾在二氧化锰的催化作用下会生成氧气,氧气有助燃性,
| 实验方法 | 现象 | 结论和反应的符号表达式 |
| 取少量样品于试管中,加热,然后用带火星的木条在试管口检验 | 带火星的木条复燃 | 猜想正确 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
不合理,氯酸钾也易溶于水;
| 实验方法 | 现象 | 结论和反应的符号表达式 |
| 取少量样品于试管中,加热,然后用带火星的木条在试管口检验 | 带火星的木条复燃 | 猜想正确 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
点评 本考点主要考查质量守恒定律、氧气的实验室制取方法以及实验探究等知识.本考点是中考的重要考点之一,主要出现在实验探究题中.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
14.中考前小明的午餐食谱是:主食--面包;配菜和副食--炸鸡腿、米饭、牛排、牛奶.则该午餐食谱缺乏的营养素是( )
| A. | 维生素 | B. | 脂肪 | C. | 蛋白质 | D. | 糖类 |
15.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如图: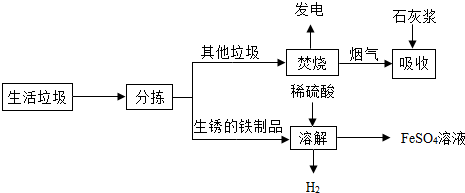
资料1:垃圾焚烧产生烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是2HCl+Ca(OH)2═CaCl2+2H2O;(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示:(仅在56.7℃或64℃温度下可同时析出两种晶体).
若需从硫酸亚铁溶液中结晶出FeSO4•4H2O,应控制的结晶温度(t)的范围为不超过64℃;
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑;
(7)请你就扬州市生活垃圾处理提一条建议生活垃圾分类回收等.

资料1:垃圾焚烧产生烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是2HCl+Ca(OH)2═CaCl2+2H2O;(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示:(仅在56.7℃或64℃温度下可同时析出两种晶体).
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑;
(7)请你就扬州市生活垃圾处理提一条建议生活垃圾分类回收等.
12.下列哪种粒子所属元素,与其他三种不属于同一周期的是( )
| A. | 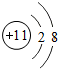 | B. | 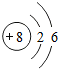 | C. | 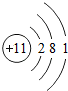 | D. | 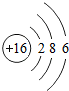 |
9.下列变化中不属于化学变化的是( )
| A. | 酒精挥发 | B. | 植物发生光合作用 | ||
| C. | 自行车出现生锈 | D. | 蜡烛燃烧 |
13.下列设计方案探究目的不能实现的是( )


| A. | 甲可探究可燃物的燃烧是否需要与氧气接触 | |
| B. | 甲可探究可燃物的燃烧是否需要达到一定的温度 | |
| C. | 乙中①③对比可探究铁的锈蚀条件与氧气是否有关 | |
| D. | 乙中①②③对比可探究铁的锈蚀条件与氧气和水是否有关 |
14.已知氢氧化钾(KOH)可溶于水,其化学性质与氢氧化钠相似,下列对氢氧化钾的化学性质的说法中错误的是( )
| A. | 能使紫色石蕊溶液变红 | B. | 能使无色酚酞溶液变红 | ||
| C. | 能与稀盐酸反应 | D. | 能与二氧化碳反应 |
 有A、B、C、D、E五种常见的物质,它们相互转化的关系如图所示,其中A、D是黑色粉末状固体,E是一种亮紫红色固体,且A、E是单质;B、C是元素组成相同的无色无味气体,且B能使澄清的石灰水变浑浊,据此,请回答下列问题:
有A、B、C、D、E五种常见的物质,它们相互转化的关系如图所示,其中A、D是黑色粉末状固体,E是一种亮紫红色固体,且A、E是单质;B、C是元素组成相同的无色无味气体,且B能使澄清的石灰水变浑浊,据此,请回答下列问题: