题目内容
今天是实验室开放的日子,小军、小华和小英三位同学利用下图所示装置在实验室制取O2和CO2,并对它们的有关性质进行研究,请回答下列问题.

(1)写出上述标号的仪器名称:① 、②
(2)小军同学用氯酸钾和二氧化锰固体制取O2,应选用上图中的 装置(填编号),该反应的化学方程式为 ;当O2收集满并取出集气瓶后,停止该实验的正确操作方法 .
(3)小华用C装置制取二氧化碳,实验原理是 .最终得到二氧化碳0.1mol,问需碳酸钙多少克?(根据化学方程式列式计算)

(1)写出上述标号的仪器名称:①
(2)小军同学用氯酸钾和二氧化锰固体制取O2,应选用上图中的
(3)小华用C装置制取二氧化碳,实验原理是
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步骤和注意点,二氧化碳的实验室制法,根据化学反应方程式的计算
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
利用加热的方法制取气体,并且用排水法收集时,要按照一定的步骤进行,特别是要注意集满气体后的操作顺序,以防发生安全事故;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
已知二氧化碳的量,可以计算反应需要碳酸钙的质量.
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
利用加热的方法制取气体,并且用排水法收集时,要按照一定的步骤进行,特别是要注意集满气体后的操作顺序,以防发生安全事故;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
已知二氧化碳的量,可以计算反应需要碳酸钙的质量.
解答:解:(1)①是长颈漏斗,通过长颈漏斗可以向锥形瓶中注入液体药品;②是锥形瓶,常用作反应容器.
故填:长颈漏斗;锥形瓶.
(2)用氯酸钾和二氧化锰固体制取需要加热,应该用B装置作为制取装置;
该反应的化学方程式为:2KClO3
2KCl+3O2↑;
当O2收集满并取出集气瓶后,停止该实验的正确操作方法是:先把导管移出水面,后熄灭酒精灯,以防水倒流入试管,把试管炸裂.
故填:B;2KClO3
2KCl+3O2↑;先把导管移出水面,后熄灭酒精灯.
(3)用C装置制取二氧化碳的实验原理是:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳.
故填:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳.
解:设需要碳酸钙的质量为x,
生成二氧化碳的质量为:44g/mol×0.1mol=4.4g,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
=
,
x=10g,
答:需要碳酸钙的质量是10g.
故填:长颈漏斗;锥形瓶.
(2)用氯酸钾和二氧化锰固体制取需要加热,应该用B装置作为制取装置;
该反应的化学方程式为:2KClO3
| ||
| △ |
当O2收集满并取出集气瓶后,停止该实验的正确操作方法是:先把导管移出水面,后熄灭酒精灯,以防水倒流入试管,把试管炸裂.
故填:B;2KClO3
| ||
| △ |
(3)用C装置制取二氧化碳的实验原理是:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳.
故填:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳.
解:设需要碳酸钙的质量为x,
生成二氧化碳的质量为:44g/mol×0.1mol=4.4g,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
| 100 |
| 44 |
| x |
| 4.4g |
x=10g,
答:需要碳酸钙的质量是10g.
点评:本题考查仪器的用途、装置的选择、化学方程式的书写、实验基本操作等方面的知识,只有综合掌握教材内容才能正确的做出解答.

练习册系列答案
相关题目
 哈尔滨在2011年加大城市建设力度,重点进行路桥建设、水源治理,届时建成“护水亲水,空气清新”“一江居中,两岸繁荣”的新型城市(如图),下列做法能造成水源污染的是( )
哈尔滨在2011年加大城市建设力度,重点进行路桥建设、水源治理,届时建成“护水亲水,空气清新”“一江居中,两岸繁荣”的新型城市(如图),下列做法能造成水源污染的是( )| A、工业“三废”经处理后排放 |
| B、大量含磷洗涤剂任意排放 |
| C、农业化肥农药合理使用 |
| D、城市生活污水处理后排放 |
乙酸乙酯(C4H8O2) 常用于食品中以增强食物的芳香性.下列关于乙酸乙酯的说法正确的是( )
| A、碳元素的质量分数为36.6% |
| B、摩尔质量为88 |
| C、碳、氢、氧三种元素质量比为2:4:1 |
| D、每个分子由4个碳原子、8个氢原子和2个氧原子构成 |

 实验室利用如图1所示装置进行加热氯酸钾制氧气的实验.
实验室利用如图1所示装置进行加热氯酸钾制氧气的实验.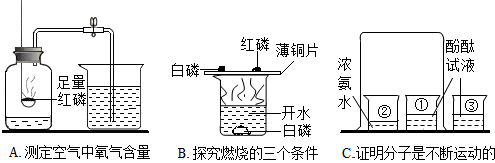
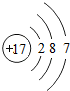 如图是氯元素的原子结构示意图,该原子的核电荷数为
如图是氯元素的原子结构示意图,该原子的核电荷数为