题目内容
17.为了测定某品牌纯碱样品中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质),兴趣小组进行了如下图所示的实验.分析并计算: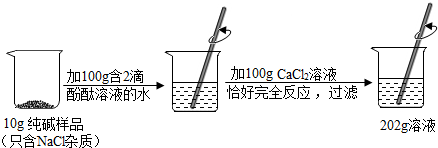
(1)恰好完成反应时可观察到的现象时刚好不再有白色沉淀生成,溶液由红色变为无色;
(2)样品中碳酸钠的质量分数(精确到0.1%).
分析 碳酸钠与氯化钙反应生成碳酸钙和氯化钠,根据质量守恒定律计算碳酸钙质量,根据碳酸钙质量结合方程式计算碳酸钠质量,进一步计算样品中碳酸钠的质量分数.
解答 解:(1)碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,所以可以看到有白色沉淀生成,恰好完成反应时可观察到的现象是:刚好不再有白色沉淀生成,溶液由红色变为无色,故填:刚好不再有白色沉淀生成,溶液由红色变成无色.
(2)由图示可知,生成碳酸钙质量的质量为10g+100g+100g-202g=8g
设碳酸钠的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 8g
$\frac{106}{x}$=$\frac{100}{8g}$
x=8.48g
样品中碳酸钠的质量分数$\frac{8.48g}{10g}$×100%=84.8%
答:样品中碳酸钠的质量分数84.8%
点评 本题难度不大,掌握根据化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出碳酸钙的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 饱和溶液不能再溶解其他溶质 | |
| B. | 饱和溶液降温一定会析出晶体 | |
| C. | 不饱和溶液变成饱和溶液,溶质质量分数一定变大 | |
| D. | 析出晶体后的溶液一定是该温度下的饱和溶液 |
5.下列化学实验基本操作中正确的是( )
| A. | 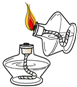 点燃酒精 | B. | 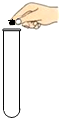 取用颗粒状固体 | C. | 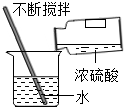 稀释浓硫酸 | D. |  给液体加热 |
2.氢氧化钠是一种重要的化工原料,也是实验室中重要的化学试剂.
(1)氢氧化钠暴露在空气中容易吸收空气中的水蒸气而潮解,还会与空气中的二氧化碳气体反应而变质,其化学反应方程式是2NaOH+CO2═Na2CO3+H2O.
(2)我校初三化学兴趣小组的同学在化学实验室整理药品时发现了一瓶久置的氢氧化钠固体,于是他们对这瓶氢氧化钠固体的成分进行了探究.
【提出问题】这瓶氢氧化钠固体是否变质?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想1:该固体没变质;
猜想2:该固体全变质;
猜想3:该固体部分变质.
设计方案并进行实验】请你与他们一起完成,并回答所给出的问题.
【反思交流】要除去久置的氢氧化钠中的杂质,所用的方法是Na2CO3+Ca(OH)2═2NaOH+CaCO3↓(用化学方程式表示).
(1)氢氧化钠暴露在空气中容易吸收空气中的水蒸气而潮解,还会与空气中的二氧化碳气体反应而变质,其化学反应方程式是2NaOH+CO2═Na2CO3+H2O.
(2)我校初三化学兴趣小组的同学在化学实验室整理药品时发现了一瓶久置的氢氧化钠固体,于是他们对这瓶氢氧化钠固体的成分进行了探究.
【提出问题】这瓶氢氧化钠固体是否变质?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想1:该固体没变质;
猜想2:该固体全变质;
猜想3:该固体部分变质.
设计方案并进行实验】请你与他们一起完成,并回答所给出的问题.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样于试管中,加水溶解,滴入过量的CaCl2溶液 | 有沉淀生成 | 猜想3正确 |
| ②反应后过滤,取上层清液,滴入 酚酞溶液 | 溶液变红 |
6.下列光关于实验现象的描述正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| C. | 硝酸铵溶解于水时,溶液温度降低 | |
| D. | 电解水时,连接电源正极与负极的玻璃管内产生气体的体积比约为2:1 |
7.如图是初中化学中的一些重要实验.下列对如图所示实验的分析,不正确的是( )
| A. | 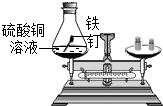 实验既可以说明铁能与硫酸铜反应,又可以验证质量守恒定律 | |
| B. | 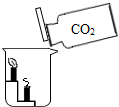 倾倒CO2时上层的蜡烛先熄灭,下层的蜡烛后熄灭 | |
| C. | 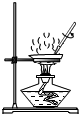 用玻璃棒搅拌的目的是防止局部受热造成液滴飞溅 | |
| D. |  集气瓶内放少量水的目的是防止溅落的溶化物炸裂瓶底 |