题目内容
12.水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用.如图为自来水厂净水过程示意图: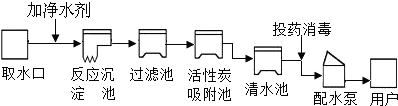
(1)如图吸附池内的活性炭吸附水中杂质属于物理变化,经沉淀、过滤等净化处理后所得的水不是纯净物(填“是”或“不是”).
(2)自来水厂常用的消毒剂有二氧化氯(ClO2)、漂白粉等.请完成工业上制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(3)生活中不宜用凉开水养鱼,其主要原因是凉开水几乎不含d
a.氧元素 b.水分子 c.氧原子 d.氧分子
(4)家庭生活中可以用肥皂水检验某水样是硬水还是软水,可用煮沸方法降低水的硬度.
(5)有些科学家预言:“世界上最后一滴水就是人类的眼泪”.这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染.请你举一例节约用水的做法:用淘米水浇花等.
分析 (1)分析活性炭在自来水生产过程中的作用;并判断经沉淀、过滤后的水是不是纯净物;
(2)利用质量守恒定律中元素守恒、原子守恒来分析解答;
(3)根据氧气可以供给呼吸解答;
(4)生活中将硬水转化为软水的常用方法是煮沸,常用肥皂水区分硬水和软水;
(5)举例说明节约用水的方法.
解答 解:
(1)活性炭具有疏松多孔结构,能吸附有毒、色素、异味等物质,在自来水生产中起到吸附水中有毒有味物质的作用;属于物理变化;经沉淀、过滤的水只是除去了水中不溶性固体杂质,仍含有许多可溶性物质,所以得到的不是纯净物;
(2)由化学方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+X
根据质量守恒定律可知,反应前后的原子个数是相等的,
反应前有2个钙原子,则反应后也有2个钙原子,反应前共4个氯原子,则反应后也有4个氯原子,反应前共有4个氧原子,则反应后也应有4个氧原子,则X中应含有4个氢原子和2个氧原子;即X的化学式为H2O.
(3)氧气可以供给呼吸,氧气是由氧分子构成的,生活中不宜用凉开水养鱼,其主要原因是凉开水几乎不含氧分子;
(4)生活中将硬水转化为软水的常用方法是煮沸,软水中滴入肥皂水会产生丰富的泡沫,而硬水滴入肥皂水产生的泡沫很少且有浮渣,所以常用肥皂水来检验某水样是硬水还是软水;
(5)节约用水应从每个人做起,可结合生活中的具体事例来说明如何节约用水,如一水多用、及时关闭水龙头、用淘米水浇花、农业浇灌改大水漫灌为喷灌等;
故答案为:(1)物理;不是;(2)H2O;+4;(3)d;(4)肥皂水;煮沸;(5)用淘米水浇花等.
点评 掌握净化水的方法,硬水软化、鉴别等知识才能结合具体情景灵活分析解答.

练习册系列答案
相关题目
7.阳新盛产茶叶,茶叶中含有茶氨酸(化学式为C7H14O3N2)、锌、硒等多种成分,茶树适宜在pH为5-6的土壤中生长,下列说法不正确的是( )
| A. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 茶氨酸属于有机物,锌、硒指单质 | |
| C. | 一个茶氨酸分子中含有3个氧原子 | |
| D. | 茶树不宜在碱性土壤中生长 |
8.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 为了身体健康,必须均衡膳食 | |
| B. | 为预防缺碘性疾病,可食用适量海带 | |
| C. | 为延长食品保质期,在食品中添加大量的防腐剂 | |
| D. | 为使馒头、面包等发面食品松软可口,制作时可添加适量碳酸氢钠 |
7.“食品安全”是健康的前提,下列做法可行的是( )
| A. | 用甲醛浸泡海鲜 | B. | 在果汁中加入“塑化剂”增加口感 | ||
| C. | 用工业盐(亚硝酸钠)腌制食品 | D. | 在煲好的鸡汤中加入碘盐 |
4.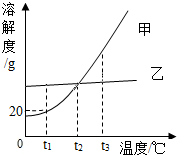 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | 甲的溶解度比乙的溶解度大 | |
| B. | t1℃时,100g甲饱和溶液中溶质的质量是20g | |
| C. | t2℃时,甲、乙的两种饱和溶液中溶质的质量分数相等 | |
| D. | 将等质量甲、乙的两种溶液分别由t1℃降至t2℃,析出甲的质量一定比析出乙的质量大 |
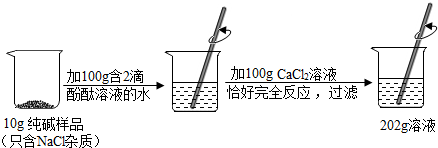
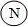 ”和“
”和“ ”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题:
”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题: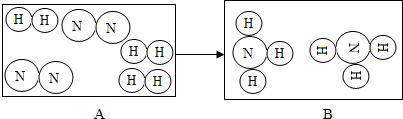
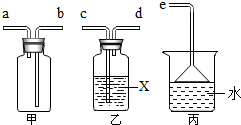 SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.
SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.