题目内容
20.某化学兴趣小组利用下列装置进行O2的实验室制法和有关性质的研究.实验室提供以下常用仪器,供完成下列气体制取实验时选用(不可重复选用).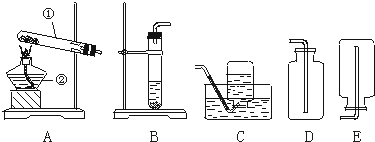
(1)过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体,它在土豆块的催化作用下能迅速分解,放出氧气.小玲同学采用该反应原理制取氧气,她应选择的发生装置是B收集装置是C或D(写出装置的代号).
(2)小丽同学打算自己探究一下MnO2在分解过氧化氢时所起的作用,但手边没有现成的MnO2药品,只有高锰酸钾,30%过氧化氢溶液、木条、水、火柴.若要先得到MnO2粉末,可选用的发生装置是A(写出装置的代号),写出反应的化学式表达式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;.反应类型是分解反应.
分析 (1)根据双氧水分解的反应原理及氧气的密度和溶解性确定发生和收集装置;
(2)根据高锰酸钾制氧气属于固体和固体加热制氧气解答.
解答 解:(1)过氧化氢无色溶液(溶质为H2O2),在二氧化锰作催化剂的条件下反应来制取氧气,不需加热,属于“固液常温型”,故选择的发生装置是B;
氧气不易溶于水且比空气的密度大所以可用排水法或向上排空气法收集,即选择C或D装置收集;
(2)高锰酸钾分解可以产生二氧化锰,高锰酸钾分解产生氧气属于固体和固体加热制氧气,故选发生装置A;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应由一种物质反应生成三种物质,符合分解反应“一变多”的特征,属于分解反应.
故答案为:(1)B; C或D;
(2)A;2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;分解反应.
点评 本题考查了实验室依据双氧水制取氧气的反应原理判断制取氧气的发生装置,依据气体的密度和溶解性判断收集装置,难度不大,掌握方法即可正确解答.

练习册系列答案
相关题目
15.主要为人体提供蛋白质的食物是( )
| A. |  白菜 | B. |  香蕉 | C. |  鲜鱼 | D. |  黄瓜 |
8.被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.某实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体.请回答有关问题:
(1)填写上表只有关内容.
(2)写出B试管中发生反应的符号表达式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入 A、B两个试管中. ②分别向A、B两试管中同时加入等质量 (少量)的二氧化锰,观察现象.  | A试管中无明显现象 B试管中有气泡 产生 | A试管中的无色液 体是水. B试管中的无色液体是双氧水. |
(2)写出B试管中发生反应的符号表达式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.
5.下列物质中不会造成空气污染的是( )
| A. | 可吸入颗粒 | B. | 二氧化氮 | C. | 氧气 | D. | 二氧化硫 |
12.某农科院葡萄基地培育的“无核”紫葡萄中,含有丰富的白藜芦醇(C14H12O3),它具有抗癌性,能抑制癌细胞的增生.下列有关白藜芦醇的计算,正确的是( )
| A. | 其相对分子质量的计算式为12×14×1×12×16×3 | |
| B. | 分子中碳、氢、氧三种元素的原子个数比为14:12:3 | |
| C. | 物质中碳、氢、氧三种元素的质量比为14:1:8 | |
| D. | 其相对分子质量为200 |