题目内容
6.某同学在实验室用氯化钠固体和蒸馏水配制500g溶质质量分数为0.9%的生理盐水时,涉及以下操作:①称量 ②溶解 ③计算 ④装入试剂瓶贴好标签.配制上述溶液的操作顺序是③①②④(填序号),需氯化钠的质量为4.5g.分析 根据配制溶质质量分数一定的溶液的基本步骤,溶质质量=溶液质量×溶质的质量分数进行分析解答.
解答 解:配制60g溶质质量分数为5%的NaCl溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶,故正确的操作顺序是③①②④;需要氯化钠的质量是:500g×0.9%=4.5g;
故答案为:③①②④;4.5g.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、溶质的质量=溶液质量×溶质的质量分数是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.关于空气中某些成分用途的说法,正确的是( )
| A. | 氧气既支持呼吸,又支持燃烧,是一种有百利而无一害的气体 | |
| B. | 二氧化碳能供给植物呼吸,使植物长得繁茂 | |
| C. | 灯泡中充入氮气,能增加灯泡的亮度 | |
| D. | 利用稀有气体中氙气的特有性质,能制成车用氙气大灯 |
17.如表是几种家用清洁剂的功能和有效成分
据表回答下列问题:
(1)“洁厕灵”与马桶中污垢(主要成分为CaCO3)反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)在盛有少量二氧化锰的试管中,加入少量“活性彩漂”液体,观察到的现象是有大量气泡产生;
(3)“洁厕灵”与“漂白精”混合易产生一种气体X,反应的化学方程式为:NaClO+2HCl═NaCl+X↑+H2O,则X的化学式是Cl2,由此得出的一条生活经验是“洁厕灵”与“漂白精”不能混合使用.
| 清洁剂名称 | 洁厕灵 | 活性彩漂 | 漂白精 |
| 功能 | 清除马桶内的污垢 | 漂洗衣物,色彩更亮丽 | 快速漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO(次氯酸钠) |
(1)“洁厕灵”与马桶中污垢(主要成分为CaCO3)反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)在盛有少量二氧化锰的试管中,加入少量“活性彩漂”液体,观察到的现象是有大量气泡产生;
(3)“洁厕灵”与“漂白精”混合易产生一种气体X,反应的化学方程式为:NaClO+2HCl═NaCl+X↑+H2O,则X的化学式是Cl2,由此得出的一条生活经验是“洁厕灵”与“漂白精”不能混合使用.
14.下列是四种粒子的结构示意图,一个说法中正确的是( )


| A. | 它们表示四种元素 | B. | ④属于阴离子 | ||
| C. | ③的元素在化合物中显+1价 | D. | ①和②的化学性质相似 |
1.下列为常见物质的pH,呈碱性的是( )
| A. |  牙膏pH=8.1 | B. |  食醋pH=2.2 | C. |  橙子pH=3.2 | D. |  苹果pH=4.0 |
11. 如图所示,上、下两个广口瓶分别装有空气和二氧化氮气体,中间用玻璃板隔开,抽取玻璃后( )
如图所示,上、下两个广口瓶分别装有空气和二氧化氮气体,中间用玻璃板隔开,抽取玻璃后( )
 如图所示,上、下两个广口瓶分别装有空气和二氧化氮气体,中间用玻璃板隔开,抽取玻璃后( )
如图所示,上、下两个广口瓶分别装有空气和二氧化氮气体,中间用玻璃板隔开,抽取玻璃后( )| A. | 空气和二氧化氮将同时向对方扩散 | |
| B. | 空气向下方扩散,二氧化氮不会向上方扩散 | |
| C. | 二氧化氮向上方扩散,空气不会向下方扩散 | |
| D. | 当两种气体分布均匀后,分子就不会向上或向下运动了 |
18. 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)【实验准备】
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
表中的现象Ⅰ为有气泡产生,现象Ⅱ对应反应的化学方程式为Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
(2)【实验过程】证明反应生成了Na2CO3
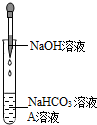
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.(1)【实验准备】
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)【实验过程】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
19.有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成,为检验其中的成分,经实验得到如表,请完成相关内容.
| 实验步骤及现象 | 结论 |
| (1)将少许白色粉末溶于水得到无色溶液A | 白色粉末中一定没有CuSO4(填化学式) |
| (2)在A中加入足量硝酸钡溶液,生成白色沉淀B,过滤得滤液C (3)在白色沉淀B中加入足量稀硝酸,现象:①白色沉淀部分溶解;②有气泡产生 (4)在滤液C中加入硝酸银溶液,生成的白色沉淀不溶于稀硝酸 | 白色粉末中一定有硫酸钠、碳酸钠和氯化钠 |