题目内容
18.根据下列A-D的四个实验,请按要求填空: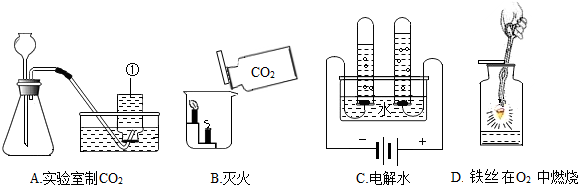
(1)A实验中,请写出标号为①的仪器名称集气瓶,实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,指出用该装置来制取二氧化碳气的一个明显错误的地方是收集方法错误.
(2)B实验中观察到的现象是蜡烛由下到上逐渐熄灭.
(3)C实验中正极产生的气体是O2(写化学式),由此实验得出水是由氢元素、氧元素组成的.
(4)D实验中如果铁丝在氧气中没有燃烧,可能的一种原因是收集的氧气不纯.
分析 (1)根据发生装置选择反应的原理和药品.根据气体密度和溶解性选择发生装置;
(2)根据二氧化碳密度大,不燃烧、不支持燃烧解答;
(3)根据电解水的实验解答;
(4)根据铁在纯净的氧气中燃烧会生成四氧化三铁进行分析.
解答 解:(1)仪器①名称为集气瓶;实验室制取二氧化碳所用药品是大理石(或石灰石)和稀盐酸,二氧化碳密度大于空气,能溶于水,故只能用向上排空气法收集,图中的收集方法错误;由于氧气不易溶于水,可以用该方法收集;
(2)把二氧化碳倒入梯形蜡烛的烧杯中观察到的现象是蜡烛由下到上逐渐熄灭;
(3)电解水,正氧负氢,故正极产生的是氧气,该实验证明了水是由氢元素和氧元素组成的;
(4)铁在纯净的氧气中燃烧会生成四氧化三铁,所以如果铁丝在氧气中没有燃烧,可能的一种原因是收集的氧气不纯.
故答案为:(1)集气瓶,CaCO3+2HCl═CaCl2+H2O+CO2↑,收集方法错误;
(2)蜡烛由下到上逐渐熄灭;
(3)O2,氢元素和氧元素;
(4)收集的氧气不纯.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
20.除去下列物质中的杂质,所选用的方法错误的一组是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CO2 | CO | 点燃 |
| B | NaCl溶液 | 泥沙 | 过滤 |
| C | CaCl2溶液 | 盐酸 | 加过量的CaCO3,过滤 |
| D | H2O | Ca2+、Mg2+ | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
9.如图所示图象与叙述对应不正确的是( )
| A. |  将质量相等且足量的锌粉和铁粉,分别投入相同质量、相同溶质质量分数的稀盐酸中 | |
| B. |  将一种稀硫酸均分成两份,分别向其中投入足量的氧化锌和碳酸锌 | |
| C. |  逐滴向一定量的氢氧化钠溶液中滴加稀盐酸直至过量 | |
| D. |  不断向稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 |
13. 如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )
如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )
 如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )
如图是炼铁的模拟实验示意图,该反应的化学方程式Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,下列有关说法错误的是( )| A. | 该实验可以观察到红色粉末变黑 | |
| B. | 待氧化铁完全反应,先停止通一氧化碳,后停止加热 | |
| C. | 氧化铁与一氧化碳的反应须在没有氧气的环境中进行 | |
| D. | 放置点燃的酒精灯目的是消除一氧化碳对环境的影响 |
3.实验室中有一瓶久置的熟石灰,同学们猜想瓶子熟石灰可能已变质,他们通过以下实验测定了其中氢氧化钙的质量分数.取10g熟石灰样品于一只洁净的烧杯中,向其中逐滴滴加15%的稀盐酸至不再产生气泡,测得加入的盐酸与烧杯中物质的质量关系如表.
(1)实验中若要用36.5%的浓盐酸(密度:1.2g/ml),配置15%的稀盐酸30g,需要36.5%的浓盐酸的体积为10.3mL.(精确到0.1)
(2)生成二氧化碳的质量为1.1g.
(3)计算样品中氢氧化钙的质量分数.
| 加入稀盐酸的质量 | 0 | 10 | 20 | 30 |
| 烧杯中物质的质量 | 10 | 19.8 | 28.9 | 38.9 |
(2)生成二氧化碳的质量为1.1g.
(3)计算样品中氢氧化钙的质量分数.
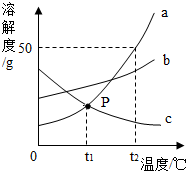 如图是a,b,c三种物质的溶解度曲线,回答下列问题:
如图是a,b,c三种物质的溶解度曲线,回答下列问题: