题目内容
18.在不用指示剂的条件下,欲将含有盐酸的氯化钙溶液由酸性变为中性,下列物品中最适宜的是( )| A. | 澄清石灰水 | B. | 硝酸银溶液 | C. | 生石灰粉末 | D. | 石灰石粉末 |
分析 根据在不用指示剂的情况下,要把含盐酸的氯化钙溶液由酸性变为中性的氯化钙溶液,也就是除去盐酸,可选碱或碳酸盐,但是在选择时不用指示剂,所以必须自己能控制溶液的酸碱性,进行分析判断.
解答 解:A、石灰水能与盐酸反应生成氯化钙和水,若不用指示剂,不好判断反应是否恰好进行,容易引入新的杂质氢氧化钙,故错误;
B、硝酸银会与盐酸、氯化钙反应,不符合除杂的原则,故错误;
C、生石灰能与盐酸反应生成氯化钙和水,过量的生石灰能与水反应生成氢氧化钙,若不用指示剂,不好判断反应是否恰好进行,容易引入新的杂质氢氧化钙,故错误;
D、盐酸能与过量的石灰石粉末反应生成氯化钙、水和二氧化碳,再过滤除去过量的难溶于水的石灰石,能除去杂质且没有引入新的杂质,符合除杂原则,故正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6. 课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
 课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )| A. | 外界大气压偏大 | B. | 实验装置可能漏气 | ||
| C. | 实验中所取的红磷过量 | D. | 集气瓶中预先未加入一定量的水 |
13.下列除去杂质的方法中,正确的是( )
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl溶液(Na2CO3) | 加入过量的Ca(NO3)2溶液、过滤 |
| B | CaO(CaCO3) | 加水、过滤 |
| C | Cu(Fe) | 加过量H2SO4溶液、过滤 |
| D | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
10.下列现象或方法,不只与空气中的水蒸气有关的是( )
| A. | 浓硫酸露置于空气中会增重、变稀 | |
| B. | 固体烧碱要密封保存 | |
| C. | 夏季空调冷气吹到的地方可看到有“冷气雾” | |
| D. | 打开浓盐酸的瓶盖,瓶口产生白雾 |
7.由石灰石、水、纯碱为原料制烧碱,发生反应的类型不包括( )
| A. | 分解反应 | B. | 置换反应 | C. | 化合反应 | D. | 复分解反应 |
8.化学工业的飞速发展给我们的生活带来了许多便利,但是一些不合理行为也给环境带来了严重的污染.下列行为不会污染环境的是( )
| A. | 回收废旧塑料减少白色污染 | |
| B. | 提倡使用私家车出行 | |
| C. | 大量使用化肥农药提高农作物的产量 | |
| D. | 将工厂排放废弃的烟囱加高 |
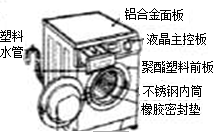 洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题.
洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题. 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.