题目内容
2.图2为某钾肥的包装标签,为检测K2SO4含量是否达标,进行如下实验:称取8.0g样品放入烧杯中,加水完全溶解后,再与足量氯化钡溶液充分反应,沉淀质量与所加氯化钡溶液质量的关系如图1所示,试通过计算判断硫酸钾的质量分数是否符合标签说明?反应化学方程式:K2SO4+BaCl2═BaSO4↓+2KCl(其他物质不参加反应).
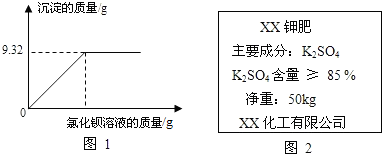
分析 从图象中看出生成的沉淀的质量是9.32g,根据硫酸钾和氢氧化钡会生成硫酸钡沉淀,利用化学方程式计算出硫酸钾的质量,再算出质量分数与标准比较从而判断是否符合包装说明;
解答 解:由图可知,生成的BaSO4质量为9.32g,设8.0g钾肥样品中含有硫酸钾的质量为x,
K2SO4+BaCl2═BaSO4↓+2KCl
174 233
x 9.32g
$\frac{174}{x}=\frac{233}{9.32g}$
解得x=6.96g
则样品中硫酸钾的质量分数为:$\frac{6.96g}{8g}$×100%=87%
由于87%>85%,该钾肥中硫酸钾的质量分数符合产品包装说明.
答案:该钾肥中硫酸钾的质量分数符合产品包装说明.
点评 该题属于标签图象型计算题,主要考查读图能力,注意解题的格式要规范.

练习册系列答案
相关题目
12.小红帮妈妈做菜时,发现妈妈将拌了嫩肉粉的肉类加入食醋腌制时产生大量气泡,引发了探究的兴趣.
【查阅资料】嫩肉粉可破坏肉质纤维结构,使肉质松软,其成分中含有碳酸氢钠(NaHCO3).小红联想已学过的碳酸钠与碳酸氢钠比较,组成元素只相差一种氢元素,决定与化学兴趣小组的同学一起,对碳酸钠和碳酸氢钠的性质的异同点进行初步探究.请你参与她们的探究活动.
【提出问题】碳酸钠和碳酸氢钠的性质有哪些相同点和不同点?
【猜想一】碳酸氢钠溶液呈碱性.
【探究实验一】
【猜想二】碳酸氢钠能与盐酸反应
【探究实验二】将气球中的碳酸氢钠粉末、碳酸钠粉末分别加入试管中,如图1所示,气球迅速胀大,说明碳酸氢钠能与盐酸发生化学反应.请写出碳酸氢钠与盐酸反应的化学反应方程式NaHCO3+HCl═NaCl+H2O+CO2↑.

【交流与讨论一】通过上述两个实验结果,小红同学得出结论:碳酸氢钠与碳酸钠的化学性质相似.其他同学对小红的结论提出质疑,认为两者组成不完全相同,化学性质应有区别.于是,兴趣小组的同学在老师的指导下,按如图2所示装置用碳酸钠和碳酸氢钠做了对比实验.
【探究实验三】碳酸钠和碳酸氢钠热稳定性.
充分加热后,现象:大试管内固体物明显变化,小试管内壁有水珠生成,试管中留下白色固体.甲烧杯中石灰水无明显现象,乙烧杯中石灰水出现白色浑浊.试回答:①在实验结束时,操作上要注意的问题是先把导管移出烧杯,后熄灭酒精灯.
②由实验可以得出的结论是碳酸氢钠热稳定性差,碳酸钠热稳定性强.
【探究实验四】到底加热后小试管中留下的这种白色固体是什么?化学兴趣小组的同学作出如下猜想①Na2CO3 ②NaOH ③Na2CO3和NaOH的混合物.为了验证她们的猜想,她们对反应后的白色固体成分进行以下实验,填写表空格.
【交流与讨论二】①实验一的结论与实验二的结论相反,在讨论时,小宇同学认为方案一的结论不正确,他的理由是碳酸钠溶液显碱性,能使酚酞试液变红色.
②设计实验二的目的是检验是否含有碳酸钠.
【探究实验五】测定嫩肉粉样品中碳酸氢钠的质量分数.兴趣小组的同学在老师的初步指导下,设计了如下实验,其主要实验步骤如下:(碱石灰为CaO和NaOH的混合物,忽略样品其他成分与盐酸的反应,装置气密性良好)
①准确称量25.0g样品放入B瓶中;②将B瓶分别与A和C相连,打开开关K,从a处缓缓鼓入空气几分钟;③将开关K关闭,再将已称量过的干燥管D与瓶C连接;④将租来稀盐酸缓缓注入B瓶中,待反应完全后,再次打开开关K缓缓鼓入空气几分钟;⑤称量干燥管D,增重11.0g.
回答:(1)A瓶的作用是除去空气中的二氧化碳.
(2)由此可测出样品中碳酸氢钠的质量分数是84%.
(3)实验测得的结果比实际偏大,可能的原因是碱石灰吸收了空气中的水蒸气和二氧化碳.(答一种即可)
【查阅资料】嫩肉粉可破坏肉质纤维结构,使肉质松软,其成分中含有碳酸氢钠(NaHCO3).小红联想已学过的碳酸钠与碳酸氢钠比较,组成元素只相差一种氢元素,决定与化学兴趣小组的同学一起,对碳酸钠和碳酸氢钠的性质的异同点进行初步探究.请你参与她们的探究活动.
【提出问题】碳酸钠和碳酸氢钠的性质有哪些相同点和不同点?
【猜想一】碳酸氢钠溶液呈碱性.
【探究实验一】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量碳酸氢钠于试管中,加适量水溶解, 再滴入几滴无色酚酞试液 | 无色酚酞试液变红色 | 猜想一正确 |
【探究实验二】将气球中的碳酸氢钠粉末、碳酸钠粉末分别加入试管中,如图1所示,气球迅速胀大,说明碳酸氢钠能与盐酸发生化学反应.请写出碳酸氢钠与盐酸反应的化学反应方程式NaHCO3+HCl═NaCl+H2O+CO2↑.

【交流与讨论一】通过上述两个实验结果,小红同学得出结论:碳酸氢钠与碳酸钠的化学性质相似.其他同学对小红的结论提出质疑,认为两者组成不完全相同,化学性质应有区别.于是,兴趣小组的同学在老师的指导下,按如图2所示装置用碳酸钠和碳酸氢钠做了对比实验.
【探究实验三】碳酸钠和碳酸氢钠热稳定性.
充分加热后,现象:大试管内固体物明显变化,小试管内壁有水珠生成,试管中留下白色固体.甲烧杯中石灰水无明显现象,乙烧杯中石灰水出现白色浑浊.试回答:①在实验结束时,操作上要注意的问题是先把导管移出烧杯,后熄灭酒精灯.
②由实验可以得出的结论是碳酸氢钠热稳定性差,碳酸钠热稳定性强.
【探究实验四】到底加热后小试管中留下的这种白色固体是什么?化学兴趣小组的同学作出如下猜想①Na2CO3 ②NaOH ③Na2CO3和NaOH的混合物.为了验证她们的猜想,她们对反应后的白色固体成分进行以下实验,填写表空格.
| 实验操作 | 实验现象 | 实验结论 |
| 实验一:取少量反应后的白色固体溶于水, 滴几滴无色酚酞试液 | 溶液变成红色 | 白色固体一定是NaOH |
| 实验二:取少量反应后的白色固体溶于水, 加入过量氯化钙溶液 | 产生白色沉淀 | 白色固体含有Na2CO3 |
| 实验三:取实验二所得的上层清液于试管中, 滴加几滴无色酚酞试液 | 无色酚酞试液不变色 | 白色固体是Na2CO3,而不是NaOH |
②设计实验二的目的是检验是否含有碳酸钠.
【探究实验五】测定嫩肉粉样品中碳酸氢钠的质量分数.兴趣小组的同学在老师的初步指导下,设计了如下实验,其主要实验步骤如下:(碱石灰为CaO和NaOH的混合物,忽略样品其他成分与盐酸的反应,装置气密性良好)
①准确称量25.0g样品放入B瓶中;②将B瓶分别与A和C相连,打开开关K,从a处缓缓鼓入空气几分钟;③将开关K关闭,再将已称量过的干燥管D与瓶C连接;④将租来稀盐酸缓缓注入B瓶中,待反应完全后,再次打开开关K缓缓鼓入空气几分钟;⑤称量干燥管D,增重11.0g.
回答:(1)A瓶的作用是除去空气中的二氧化碳.
(2)由此可测出样品中碳酸氢钠的质量分数是84%.
(3)实验测得的结果比实际偏大,可能的原因是碱石灰吸收了空气中的水蒸气和二氧化碳.(答一种即可)
17.以下是一个化学反应的微观示意图.从该示意图中获取的信息正确的是( )


| A. | 反应前后元素种类发生改变 | |
| B. | 该反应的基本类型是化合反应 | |
| C. | 反应前后分子种类不发生改变 | |
| D. | 参加反应的两种分子的个数比是1:2 |


