题目内容
大理石是一种常用的建筑材料,现在也常用于家庭装修中.我省云浮市盛产大理石,是为测定该市某地大理石中碳酸钙的质量分数(假设杂质不参加反应,且不溶于水),我市某中学化学兴趣小组设计了以下二个实验方案:
方案I:①称取10g大理石样品;②先将其高温煅烧至质量不再改变,然后把剩余的固体放在密闭干燥容器中,并冷却至室温,称得剩余固体的质量为6.04g.
方案Ⅱ:①称取10g大理石样品;②将其加入足量的稀盐酸中,使碳酸钙全部溶解;③用导气管将生成的气体通入过量的澄清石灰水中;④将步骤③中生成的沉淀过滤、洗涤、干燥,称知沉淀的质量8.8g.
回答下列问题:
(1)在方案I中冷却剩余的固体为什么要在密闭、干燥的容器中进行?
(2)小聪同学根据方案I计算碳酸钙质量分数的过程如下:
设大理石中碳酸钙的质量为x,则依
CaCO3
CaO+CO2↑
100 56
x 6.04g
解得x=10.78
进而知,ω(CaCO3)=
×100%=107.8%
小聪同学的得出的结果明显不符合实际,你认为小聪同学错在那里? 请写出你的计算方法:
(3)通过对二个方案中碳酸钙质量分数的计算可知,由方案II算出的碳酸钙的质量分数要比方案I低,你认为其中可能的原因是 (填序号)
A.生成的二氧化碳有一部分溶于水
B.装置的气密性不好,有部分二氧化碳逸出
C.生成的沉淀不应该洗涤和干燥
D.导管中仍有一部分二氧化碳未排出
(4)小明同学也自己设计了一个实验方案来测定大理石中碳酸钙的质量分数.方案如下:
①称取10g大理石样品于烧杯(烧杯的质量为120克)中;
②将其加入100克的稀盐酸中,使碳酸钙全部溶解;
③
④根据质量守恒定律,将所得数据处理后得到二氧化碳的质量.
方案I:①称取10g大理石样品;②先将其高温煅烧至质量不再改变,然后把剩余的固体放在密闭干燥容器中,并冷却至室温,称得剩余固体的质量为6.04g.
方案Ⅱ:①称取10g大理石样品;②将其加入足量的稀盐酸中,使碳酸钙全部溶解;③用导气管将生成的气体通入过量的澄清石灰水中;④将步骤③中生成的沉淀过滤、洗涤、干燥,称知沉淀的质量8.8g.
回答下列问题:
(1)在方案I中冷却剩余的固体为什么要在密闭、干燥的容器中进行?
(2)小聪同学根据方案I计算碳酸钙质量分数的过程如下:
设大理石中碳酸钙的质量为x,则依
CaCO3
| ||
100 56
x 6.04g
解得x=10.78
进而知,ω(CaCO3)=
| 10.78 |
| 10g |
小聪同学的得出的结果明显不符合实际,你认为小聪同学错在那里?
(3)通过对二个方案中碳酸钙质量分数的计算可知,由方案II算出的碳酸钙的质量分数要比方案I低,你认为其中可能的原因是
A.生成的二氧化碳有一部分溶于水
B.装置的气密性不好,有部分二氧化碳逸出
C.生成的沉淀不应该洗涤和干燥
D.导管中仍有一部分二氧化碳未排出
(4)小明同学也自己设计了一个实验方案来测定大理石中碳酸钙的质量分数.方案如下:
①称取10g大理石样品于烧杯(烧杯的质量为120克)中;
②将其加入100克的稀盐酸中,使碳酸钙全部溶解;
③
④根据质量守恒定律,将所得数据处理后得到二氧化碳的质量.
考点:实验探究物质的组成成分以及含量,盐的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:(1)根据石灰石高温煅烧后生成物的性质进行分析;
(2)根据二氧化碳的质量,可求参加反应的碳酸钙的质量,从而可求石灰石中碳酸钙的质量分数.
(3)方案Ⅲ是根据生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,其中生成二氧化碳质量是关键;
(4)根据杂质不参加反应,且不溶于水,来设计实验.
(2)根据二氧化碳的质量,可求参加反应的碳酸钙的质量,从而可求石灰石中碳酸钙的质量分数.
(3)方案Ⅲ是根据生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,其中生成二氧化碳质量是关键;
(4)根据杂质不参加反应,且不溶于水,来设计实验.
解答:解:(1)石灰石高温煅烧后生成氧化钙和二氧化碳,氧化钙能吸收空气中的水分,冷却时要在密闭干燥容器中进行;
(2)因为剩余固体质量6.04g包含了杂质质量,所以得出碳酸钙的质量分数超过100%;
生成二氧化碳质量=10g-6.04g=3.96g,
设生成3.96g二氧化碳,需碳酸钙质量为x
CaCO3
CaO+CO2↑
100 44
x 3.96g
=
x=9g
CaCO3%=
×100%=90%
(3)方案Ⅲ是:根据生成的二氧化碳与氢氧化钙反应,生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,而二氧化碳溶于水且导管中仍有部分二氧化碳未导出,计算得出的碳酸钙质量分数要比方案工和方案Ⅱ低,故选:AB;
(4)杂质不参与反应,且不溶于水设计实验:
实验步骤:①称取石灰石样品;
②加入足量的盐酸,使碳酸钙全部溶解;
③过滤、洗涤、干燥,称量不溶物(即杂质)的质量;
④根据质量守恒定律,将所得数据处理后得到二氧化碳的质量.
故答案为:
(1)因为剩余固体中的氧化钙能吸收空气中的水分;
(2)剩余固体质量6.04g包括了杂质的质量,90%;
(3)AB;
(4)过滤、洗涤、干燥,称量不溶物(即杂质)的质量.
(2)因为剩余固体质量6.04g包含了杂质质量,所以得出碳酸钙的质量分数超过100%;
生成二氧化碳质量=10g-6.04g=3.96g,
设生成3.96g二氧化碳,需碳酸钙质量为x
CaCO3
| ||
100 44
x 3.96g
| 100 |
| x |
| 44 |
| 3.96g |
x=9g
CaCO3%=
| 9g |
| 10g |
(3)方案Ⅲ是:根据生成的二氧化碳与氢氧化钙反应,生成碳酸钙质量来计算石灰石中碳酸钙的质量分数,而二氧化碳溶于水且导管中仍有部分二氧化碳未导出,计算得出的碳酸钙质量分数要比方案工和方案Ⅱ低,故选:AB;
(4)杂质不参与反应,且不溶于水设计实验:
实验步骤:①称取石灰石样品;
②加入足量的盐酸,使碳酸钙全部溶解;
③过滤、洗涤、干燥,称量不溶物(即杂质)的质量;
④根据质量守恒定律,将所得数据处理后得到二氧化碳的质量.
故答案为:
(1)因为剩余固体中的氧化钙能吸收空气中的水分;
(2)剩余固体质量6.04g包括了杂质的质量,90%;
(3)AB;
(4)过滤、洗涤、干燥,称量不溶物(即杂质)的质量.
点评:本题是运用化学中的基本思想质量守恒思想,通过归纳碳酸钙在不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关氧气的说法错误的是( )
| A、氧气能使带火星的木条复燃 |
| B、木炭在氧气中燃烧,发出明亮白光 |
| C、硫在氧气中燃烧发出微弱的淡蓝色火焰,生成刺激性气味的气体 |
| D、物质与氧气发生的反应都是氧化反应 |
实验是学习化学的重要途径.下列实验操作中正确的是( )
A、 称量氯化钠 |
B、 制取二氧化碳 |
C、 加热氯酸钾制氧气 |
D、 测定溶液的pH |
如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | N2 | O2 | 将气流通过灼热的铜网 |
| B | CO2 | CO | 将混合气体点燃 |
| C | Cu | C | 在空气中充分灼烧 |
| D | Cu | Fe2O3 | 通入CO,高温 |
| A、A | B、B | C、C | D、D |
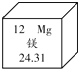 镁有“国防金属”的美誉.在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
镁有“国防金属”的美誉.在元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )| A、原子序数为12 |
| B、元素符号为Mg |
| C、原子核外电子数为24 |
| D、相对原子质量为24.31 |
化学与我们的身体健康息息相关,下列有关说法中,不合理的是( )
| A、变质食品中常含有霉菌毒素,不可食用 |
| B、使用甲醛浸泡银鱼,可防止银鱼腐烂 |
| C、少年儿童不能盲目吃各种营养补品 |
| D、为了自己和他人的健康,拒绝烟草,远离毒品 |
下列化学方程式书写正确的是( )
A、4Fe+3O2
| ||||
B、2H2+O2
| ||||
| C、CaO+H2O=Ca(OH)2 | ||||
| D、CuSO4+H2O=CuSO4?5H2O |
 为探究碱的性质,进行如下实验.
为探究碱的性质,进行如下实验.