题目内容
2.将氯化钠和碳酸钠的混合物33.8g放入125g稀盐酸中,恰好完全反应生成氯化钠和二氧化碳,得二氧化碳气体8.8g.请计算:(1)混合物中氯化钠的质量;
(2)混合物中碳酸钠的质量;
(3)求原稀盐酸中HCl的质量分数.
分析 根据二氧化碳的质量算出碳酸钠的质量和HCl的质量,进而求出氯化钠的质量和进原稀盐酸中HCl的质量分数行解答;
解答 解:(1)设要生成8.8g二氧化碳气体,需要参加反应的碳酸钠的质量为x,HCl的质量为y,则:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 8.8g
$\frac{106}{x}=\frac{73}{y}=\frac{44}{8.8g}$
解得x=21.2g
y=14.6g
原混合物中氯化钠的质量=33.8g-21.2g=12.6g;
(2)混合物中碳酸钠的质量21.2g;
(3)原稀盐酸中HCl的质量分数$\frac{14.6g}{125g}×100%$=11.68%
答:(1)原混合物中氯化钠的质量为12.6g;
(2)混合物中碳酸钠的质量21.2g;
(3)原稀盐酸中HCl的质量分数11.68%.
点评 本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小,主要是关于溶液的计算.

练习册系列答案
相关题目
20.在CuSO4和ZnSO4的混合溶液中,加入足量的铁粉,充分反应后铁粉有剩余,则反应后的溶液中含有的金属阳离子是( )
| A. | Zn2+ | B. | Cu2+、Fe2+ | C. | Zn2+、Fe2+ | D. | Fe2+ |
13.化学是一门以实验为基础的科学,正确的实验操作是完成实验任务的保证.下列实验操作中,正确的是( )
| A. |  称量固体的质量 | B. |  向试管中倾倒液体 | ||
| C. |  验证二氧化磷的水溶液显酸性 | D. |  测定溶液的pH |
17.小红、小军、小明三人化学学习小组在实验中,用到了三个分别盛有KCl溶液、KOH溶液、K2SO4溶液的滴瓶.
小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行了如下探究.
提出问题:该滴瓶中溶质的成分是什么?
提出猜想:通过分析,提出如下猜想:
猜想Ⅰ溶质成分只有:KCl;
猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为:KCl、K2SO4;
猜想Ⅳ溶质成分为:KCl、KOH和K2SO4.
实验探究:为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
实验反思:小明认为该实验方案并未证明猜想Ⅱ、Ⅲ是否成立,应补充相应实验予以证明,你是否赞同?否(选填“是”或“否”).
小军发现小红将三个滴瓶中的三只滴管混用,认为小红实验操作不规范,滴瓶中的试剂会因此受污染而无法再次使用,学习小组就盛有KCl溶液的滴瓶是否被另外两种试剂污染进行了如下探究.
提出问题:该滴瓶中溶质的成分是什么?
提出猜想:通过分析,提出如下猜想:
猜想Ⅰ溶质成分只有:KCl;
猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为:KCl、K2SO4;
猜想Ⅳ溶质成分为:KCl、KOH和K2SO4.
实验探究:为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
| 实验操作 | 实验现象 | 结论或解释 |
| (1)取该滴瓶内溶液烧了于试管中,向试管中加入适量BaCl2溶液 | 产生白色沉淀 | 该反应的化学方程式为BaCl2+K2SO4═BaSO4↓+2KCl |
| (2)将上述反应后的混合液过滤,取滤液于另一支试管中,向该试管中加入酚酞试液 | 酚酞试液变红色 | 证明猜想Ⅳ成立 |
11.下列各组物质充分混合后,不能得到溶液的是( )
| A. | 把蔗糖加入水中 | B. | 把水加入植物油中 | ||
| C. | 把碘加入酒精中 | D. | 把植物油加入汽油中 |
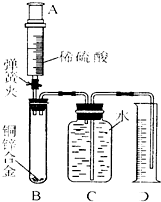 某化学小组利用图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去).探究过程如下:
某化学小组利用图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去).探究过程如下: 将10%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.请问:稀盐酸中溶质的质量分数为多少?
将10%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.请问:稀盐酸中溶质的质量分数为多少?