题目内容
14.氟、氯的相关信息如下:
下列有关这两种元素的说法中错误的是( )
| A. | 氟原子在化学反应中易得到电子形成F- | |
| B. | 氯的相对原子质量为35.45g | |
| C. | 氟、氯的化学性质相似 | |
| D. | 氟、氯都属于非金属元素 |
分析 A、根据原子结构示意图中,若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子解答;
B、根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答;
C、根据最外层电子数相同,化学性质相似解答;
D、根据氟、氯元素的汉字名称偏旁“气”可知,氟、氯元素属于非金属元素解答.
解答 解:
A、由氟原子结构示意图可知,氟原子的最外层有7个电子,在化学反应中易得到一个电子而形成带有一个单位负电荷的氟离子,离子符号为F-,故正确;
B、由题目中的元素周期表中的氯元素信息,可知氯的相对原子质量为35.45g,其单位是“1”不是“g”,通常省略不写,故错误;
C、由原子结构示意图可知,最外层电子数都为7,最外层电子数相同,化学性质相似,故正确;
D、氟、氯元素的汉字名称偏旁“气”可知,氟、氯元素属于非金属元素,故正确.
答案:B
点评 本题难度不大,了解原子结构示意图的意义、灵活运用元素周期表中元素的信息是正确解题的关键.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
5. 如图为某物质的分子模型示意图,其中“○”代表氢原子,“●”代表氧原子.下列叙述正确的是( )
如图为某物质的分子模型示意图,其中“○”代表氢原子,“●”代表氧原子.下列叙述正确的是( )
 如图为某物质的分子模型示意图,其中“○”代表氢原子,“●”代表氧原子.下列叙述正确的是( )
如图为某物质的分子模型示意图,其中“○”代表氢原子,“●”代表氧原子.下列叙述正确的是( )| A. | 此物质属于化合物 | |
| B. | 此物质的化学式为HO | |
| C. | 此物质的一个分子由4个原子构成 | |
| D. | 此物质中氢元素与氧元素的质量比是1:1 |
9.小明同学在探究氢氧化钠固体溶液的放热现象后,没有及时将盛氢氧化钠固体的试剂瓶瓶塞盖上,老师告诉小明它可能变质了.老师认为氢氧化钠固体可能变质的理由是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
小明同学对老师的说法产生了质疑,于是他设计实验方案对该固体样品进行了探究.
【提出猜想】1.该样品没有变质;2.该样品部分变质;3.该样品全部变质.
【实验探究】
【讨论交流】小刚同学认为小明同学的设计不能证明该样品一定含有氢氧化钠,理由是碳酸钠溶液呈碱性,也能使酚酞试液变红,他又补充了实验:取少量样品,加水溶解,向其中加入足量氯化钡溶液,静置,取上层清液,滴加无色酚酞溶液后溶液变红,说明该样品部分变质.
【拓展迁移】要除去部分变质的氢氧化钠溶液中的杂质,可选择氢氧化钙溶液.
小明同学对老师的说法产生了质疑,于是他设计实验方案对该固体样品进行了探究.
【提出猜想】1.该样品没有变质;2.该样品部分变质;3.该样品全部变质.
【实验探究】
| 实验编号 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取少量样品于试管里,向其中加入 稀盐酸 | 有气泡产生 | 样品变质了 |
| 2 | 取少量样品,加水溶解,然后滴加无色酚酞溶液 | 溶液变红 | 该样品部分变质 |
【拓展迁移】要除去部分变质的氢氧化钠溶液中的杂质,可选择氢氧化钙溶液.
6. 将等质量的锌粉和铁粉分别放入足量的等浓度等体积的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列说法一定正确的是( )
将等质量的锌粉和铁粉分别放入足量的等浓度等体积的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列说法一定正确的是( )
 将等质量的锌粉和铁粉分别放入足量的等浓度等体积的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列说法一定正确的是( )
将等质量的锌粉和铁粉分别放入足量的等浓度等体积的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列说法一定正确的是( )| A. | 金属活动性A>B | B. | A是铁粉,B是锌粉 | ||
| C. | 反应消耗的稀硫酸质量A=B | D. | 产生氢气质量A=B |
3.为除去下列物质中的杂质(括号内为杂质),下列操作方法能达到目的是( )
| 选项 | 物质(杂质) | 操作方法 |
| A | CO2(CO) | 将气体点燃 |
| B | CaO(CaCO3) | 加足量稀盐酸、过滤 |
| C | KNO3(NaCl) | 蒸发结晶、过滤 |
| D | FeCl2(CuCl2) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
4.甲和乙可以合成清洁燃料丙,微观过程如图.下列说法错误的是( )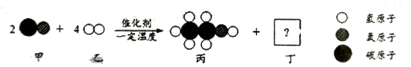

| A. | 甲中碳元素的化合价为+2价 | B. | 丙中C、H、O的质量比为12:3:8 | ||
| C. | 丁的化学式为H2O2 | D. | 该反应体现无机物可转化为有机物 |

 高压锅是生活中常用的炊具,如图是家用高压锅的示意图.
高压锅是生活中常用的炊具,如图是家用高压锅的示意图.