题目内容
20.下列是某化学小组探究物质组成与性质的实验装置图,根据要求回答:| A | B | C | D |
| 测定空气中氧气的含量 | 稀释浓硫酸 | 铁钉在空气中的变化 | 一氧化碳还原氧化铁 |
木炭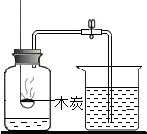 | 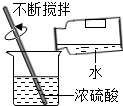 | 水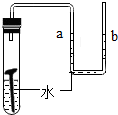 | 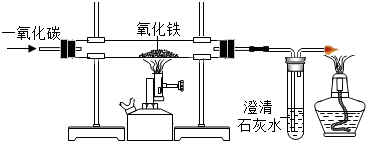 |
(2)B中玻璃棒的作用是搅拌,使产生的热量迅速扩散(加快散热);C中会出现的实验现象为铁钉生锈;U型管液面左高右低.
(3)D中硬质玻璃管内发生反应的化学方程式为3CO+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,酒精灯的作用是点燃尾气中的CO,防止污染环境.
分析 (1)A、B、C、D四个实验中:A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;而B稀释浓硫酸,应将浓硫酸倒入水中,故不能达到实验目的;A实验测定空气中氧气的含量,故应充分消耗氧气;
(2)B实验稀释浓硫酸,玻璃棒搅拌并及时散热;C实验铁丝生锈消耗空气中的氧气,管内外形成气压差,故U型管中液面左高右低;
(3)D实验一氧化碳还原氧化铁,已知反应物一氧化碳和氧化铁,生成物为二氧化碳和铁,反应条件为高温;反应完,将有尾气一氧化碳,故需要处理掉.
解答 解:
(1)经分析A、B、C、D四个实验,A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;而B稀释浓硫酸,应将浓硫酸倒入水中,故不能达到实验目的;A实验测定空气中氧气的含量,故应充分消耗氧气;
(2)B中玻璃棒的作用是搅拌、散热;一段时间后,C中的实验现象为铁丝生锈,U型管中液面左高右低;
(3)D中硬质玻璃管内发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.酒精灯的作用是点燃未反应的CO,防止其污染空气.
答案:
(1)AB;可将装置中的氧气耗尽;
(2)搅拌,使产生的热量迅速扩散(加快散热);铁钉生锈;U型管液面左高右低
(3)3CO+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2; 点燃尾气中的CO,防止污染环境.
点评 了解金属生锈的条件,探究测定空气中氧气含量的方法;掌握浓硫酸的性质和稀释方法及其注意事项;掌握一氧化碳还原氧化铁的实验原理及注意事项.

练习册系列答案
相关题目
11.要学会从化学的视角认识世界,对下列事实的解释错误的是 ( )
| 选项 | 相 关 说 法 | 解 释 |
| A | 不同种类的酸具有相似的化学性质 | 不同酸的溶液中都含有氢离子 |
| B | KMnO4溶液和K2SO4溶液的颜色不同 | 两种溶液中的阴离子不同 |
| C | H2O2 和 H2O化学性质不同 | 一个H2O2 分子比一个 H2O分子多一个氧原子 |
| D | 蔗糖溶液不导电 | 蔗糖溶液中没有自由移动的粒子 |
| A. | A | B. | B | C. | C | D. | D |
8.下列每组中的固体物质,只用水做试剂,不能将其鉴别出来的是( )
| A. | 氢氧化钠、氯化钠 | B. | 氧化铜、铁粉 | C. | 高锰酸钾、碘 | D. | 氧化钙、氢氧化钙 |
5.甲物质是种重要的有机化工原料,甲和乙反应生成丙和丁的微观示意图如图.则下列说法中正确的是( )


| A. | 乙是氧化物 | B. | 甲的化学式可能为CH2O | ||
| C. | 反应前后分子的种类、个数不变 | D. | 生成的丙、丁两物质的质量比是1:1 |
3.一种新型的甜味剂木糖醇在市场上大受欢迎.木糖醇的化学式为C5H12O5,它最大的优势是可以减少或者预防蛀牙.木糖醇的甜度与蔗糖相当,但热量只有蔗糖的60%.据介绍,木糖醇是一种原产于芬兰的天然甜味剂,后来日本从白桦树和玉米芯等植物中提炼出这种天然甜味剂.由于木糖醇不能被细菌分解,利用它来取代甜品中的糖分,可以防止蛀牙.而在口香糖里添加木糖醇是目前国际上最为普遍的防蛀方法.
(1)木糖醇是一种有机化合物(填“有机化合物”或“无机化合物”),属于营养素中的糖类,相对分子质量为152.
(2)请你设计实验证明木糖醇中含有碳元素和氢元素.
(1)木糖醇是一种有机化合物(填“有机化合物”或“无机化合物”),属于营养素中的糖类,相对分子质量为152.
(2)请你设计实验证明木糖醇中含有碳元素和氢元素.
| 操作 | 现象 | 结论 |
1.把木糖醇灼烧,再罩上一干冷的烧杯 2.迅速倒立烧杯,滴加澄清石灰水 | 烧杯内壁有水珠 石灰水变浑浊 | 木糖醇中含有氢元素 木糖醇中含有碳元素 |
 图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.
图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去. 碳及其化合物在生产、生活中应用广泛.
碳及其化合物在生产、生活中应用广泛.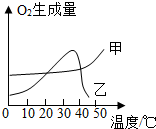 实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.
实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.