题目内容
4. 实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.
实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.现有实验材料如下:
新鲜的含过氧化氢酶3.5%的猪肝研磨液、3.5%的FeCl3溶液、新配制的3%的过氧化氢溶液.
量筒、滴管、试管、试管架、试管夹、小木条、火柴、酒精灯等.
某同学为比较过氧化氢酶和Fe3+催化效率,利用上述材料进行探究:
【提出问题】比较过氧化氢酶和Fe3+对过氧化氢分解的催化效率的高低.
【提出猜想】
猜想1:过氧化氢酶的催化效率比Fe3+高;
猜想2:Fe3+的催化效率比过氧化氢酶高;
【实验步骤】
(1)取两支洁净的试管,分别注入2ml3%的过氧化氢溶液.
(2)分别向两支试管内滴入等量的猪肝研磨液和氯化铁溶液.
(3)将带火星的小木条分别放入两支试管内液面的上方,观察现象.
【实验现象与结论】
(4)观察到滴入氯化铁溶液的试管内产生的气泡更迅速,带火星的木条易复燃,证明猜想2正确.
【继续探究】
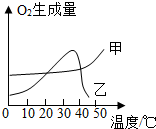
(5)该同学继续探究温度对猪肝研磨液和FeCl3溶液催化效率的影响,实验结果绘成如图,图中代表猪肝研磨液催化效果的曲线是乙,你能得到的实验结论是30~40℃时,猪肝研磨液催化效果最佳(或40℃以内,温度对FeCl3溶液催化效率几乎无影响),(写一条即可).
(6)你认为猪肝研磨液的催化效率还可能与猪肝研磨液中过氧化氢酶的浓度有关.(填一种因素即可)
分析 (1)根据实验室常用二氧化锰催化分解过氧化氢的方法制取氧气解答;
(2)根据对比新鲜的含过氧化氢酶3.5%的猪肝研磨液、3.5%的FeCl3溶液解答.
(3)根据氧气支持燃烧的性质解答;
(4)根据实验现象分析猜想解答;
(5)根据高温会破坏酶的空间结构,使酶变性失活解答;
(6)根据猪肝研磨液的催化效率还可能与猪肝研磨液中过氧化氢酶的浓度有关解答.
解答 解:
(1)实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,反应的化学方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)取两支洁净的试管,分别注入2ml3%的过氧化氢溶液.分别向两支试管内滴入等量的猪肝研磨液和氯化铁溶液;
(3)氧气支持燃烧,将带火星的小木条分别放入两支试管内液面的上方,观察现象.
(4)观察到滴入氯化铁溶液的试管内产生的气泡更迅速,带火星的木条易复燃,证明猜想2正确.
(5)该同学继续探究温度对猪肝研磨液和FeCl3溶液催化效率的影响,实验结果绘成如图,图中代表猪肝研磨液催化效果的曲线是乙;得到的实验结论是:30~40℃时,猪肝研磨液催化效果最佳(或40℃以内,温度对FeCl3溶液催化效率几乎无影响);
(6)猪肝研磨液的催化效率还可能与猪肝研磨液中过氧化氢酶的浓度有关.
答案:
(1)2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)滴入等量的猪肝研磨液和氯化铁溶液;
(3)带火星的小木条(合理即可);
(4)滴入氯化铁溶液的试管内产生的气泡更迅速,带火星的木条易复燃(合理即可).
(5)乙; 30~40℃时,猪肝研磨液催化效果最佳(或40℃以内,温度对FeCl3溶液催化效率几乎无影响)(合理即得分)
(6)猪肝研磨液中过氧化氢酶的浓度(合理即可)
点评 对于此类试题,需要考生注意的细节较多,如实验的原理、实验采用的试剂及试剂的作用、实验采用的选择、实验现象等,需要考生在平时的学习过程中注意积累.

 初中学业考试导与练系列答案
初中学业考试导与练系列答案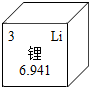 锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )
锂常被人们誉为“金属味精”,锂元素的相关信息如图,下列有关锂的说法错误的是( )| A. | 原子的核电荷数是3 | B. | 元素符号是Li | ||
| C. | 相对原子质量为6.941 | D. | 属于非金属元素 |
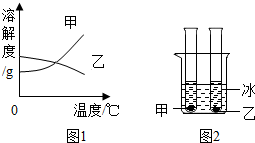 甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图1.(图2)现将两试管分别装入甲、乙两种物质室温下(20℃)的饱和溶液(试管底部均有未溶解的固体),放进盛有冰水的烧杯里,则下列说法正确的是( )| A. | 甲溶液中溶质的质量分数增大 | |
| B. | 乙试管中剩余的固体减少 | |
| C. | 试管里甲、乙两物质的溶解度都增大 | |
| D. | 试管里甲、乙两溶液中的溶质都减少 |
| A | B | C | D |
| 测定空气中氧气的含量 | 稀释浓硫酸 | 铁钉在空气中的变化 | 一氧化碳还原氧化铁 |
木炭 | 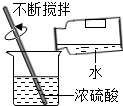 | 水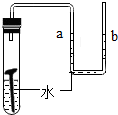 | 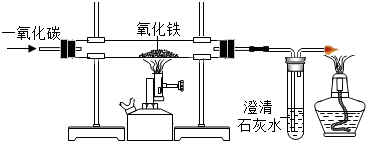 |
(2)B中玻璃棒的作用是搅拌,使产生的热量迅速扩散(加快散热);C中会出现的实验现象为铁钉生锈;U型管液面左高右低.
(3)D中硬质玻璃管内发生反应的化学方程式为3CO+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,酒精灯的作用是点燃尾气中的CO,防止污染环境.
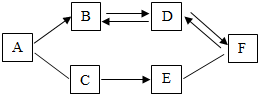 如图是初中化学中几种常见物质的反应及转化关系,A物质具有还原性,B是一种常见的气体,E的水溶液呈蓝色,如图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质,请回答:
如图是初中化学中几种常见物质的反应及转化关系,A物质具有还原性,B是一种常见的气体,E的水溶液呈蓝色,如图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质,请回答: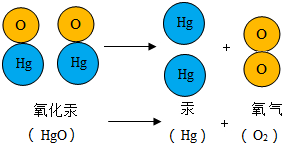 1774年,拉瓦锡用精确的定量实验研究了氧化汞分解反应中各物质质量之间的变化关系,如图是氧化汞分子分解的示意图.
1774年,拉瓦锡用精确的定量实验研究了氧化汞分解反应中各物质质量之间的变化关系,如图是氧化汞分子分解的示意图.
