题目内容
15. 金属材料在生活、生产中应用十分广泛.
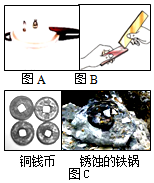
金属材料在生活、生产中应用十分广泛.(1)图A是金属的一个应用实例,利用了金属的导热性.
(2)图B是两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是比较合金和纯金属的硬度.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图C中铁制品表面的锈层可用稀酸清洗除去,写出稀盐酸除锈的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
分析 (1)图A是高压锅,据此结合金属的性质与用途进行分析解答.
(2)根据合金的性质,进行分析解答.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,写出反应的化学方程式即可.
解答 解:(1)图A是高压锅,利用了金属具有优良的导热性.
(2)图B是两块金属片相互刻划后,在纯铜片上有明显的划痕,说明合金的硬度比组成它的纯金属的硬度大,该实验探究的目的是比较合金和纯金属的硬度.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
故答案为:(1)导热;(2)比较合金和纯金属的硬度; (3)Fe2O3+6HCl═2FeCl3+3H2O.
点评 本题难度不大,掌握酸的化学性质、合金的性质、金属的性质与用途、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
5.钛在国防上有着很重要的用途.工业上常采用金属热还原法制金属钛:反应①将TiO2(或天然的金红石 )和炭粉混合加热至1000~1100K,进行氯化处理,并使生成的TiCl ,蒸气冷凝TiO2+2C+2Cl2=TiCl4+2CO;②在1070K用熔融的镁在氩气中还原TiCl4可得多孔的海绵钛 :TiCl4+2Mg=2MgC12+Ti.下列有关说法正确的是( )
| A. | 冶炼过程对环境没有污染 | |
| B. | 反应①中只有氧元素化合价没有改变 | |
| C. | 反应②属于置换反应 | |
| D. | 金属Ti在加热时不易跟氧气反应 |
20.某同学用如图装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去),在完成气密性检査后加入药品.

(1)填写表格中的空白内容:
(2)有同学认为该装罝有不足之处,请指出:该装置没有不足之处,未反应的CO进入D装置不会逸散到空气中.

(1)填写表格中的空白内容:
| 实验步骤 | 实验现象 | 实验分析 |
| ①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间 | 木炭粉减少,D中有气泡产生、澄清石灰水变浑浊且石灰水流入E烧杯中 | 此时硬质玻璃管中发生反应的化学方程式为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO |
| ②再点燃B处酒精喷灯,加热一段时间 | B处玻璃管内黑色固体变红 | 以上实验说明CO具有还原性 |
| ③停止通入二氧化碳,熄灭A、B两处的火焰 | C中有D中液体进入 | / |
4.下列化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O2 | B. | H | C. | Cu | D. | SO2 |
5.屠呦呦由于发现青蒿素获得诺贝尔奖.关于青蒿素(C15H22O5)正确的是( )
| A. | 是氧化物 | B. | 相对分子质量302克 | ||
| C. | 有42个原子 | D. | 碳元素质量分数最大 |
