题目内容
5.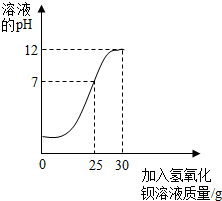 为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算:
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算:(1)生成沉淀的质量为2.33克.
(2)计算所用氢氧化钡溶液的溶质质量分数.(写出解题过程)
分析 先根据质量守恒定律求出生成沉淀硫酸钡的质量,再根据化学方程式求出氢氧化钡的质量,然后根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%即可求解.
解答 解:根据质量守恒定律,生成BaSO4质量为20g+30g-47.67g=2.33g
设参加反应的Ba(OH)2的质量为x
Ba(OH)2+H2SO4═BaSO4↓+2H2O
171 233
x 2.33g
$\frac{171}{x}=\frac{233}{2.33g}$
x=1.71g
Ba(OH)2溶液中溶质质量分数$\frac{1.71g}{25g}$×100%=6.84%
答:
(1)2.33
(2)该溶液中Ba(OH)2溶质质量分数为6.84%.
点评 解答本题关键是抓住反应前后溶液减轻的质量就是生成的沉淀硫酸钡的质量,然后结合图象得出加入的氢氧化钡质量为25g时稀硫酸和氢氧化钡恰好完全反应,只要分析清楚这两点即可较快解答该题.

练习册系列答案
相关题目
15.现有锌和另一种金属组成的合金6.5g,洋洋同学向此合金中加入100g一定溶质质量分数的稀盐酸,充分反应后发现金属完全消失,若产生氢气的质量为m.则下列判断正确的是( )
| A. | 如果合金为锌和铁,m可能是0.2g | |
| B. | 反应后溶液中的溶质只有两种 | |
| C. | 如果合金为锌和镁,m可能是0.1g,则该合金中锌的质量分数为50% | |
| D. | 如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3% |
16.利用生物发光现象可检测“超微量钙”,此处“钙”是指( )
| A. | 分子 | B. | 原子 | C. | 元素 | D. | 单质 |
20.下列有关认识错误的是( )
| A. | 常用于淡化海水的方法有蒸馏法、过滤法等 | |
| B. | 粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发 | |
| C. | 通常在苦卤中加入熟石灰制取氢氧化镁 | |
| D. | 海水中的食盐用途广泛,例如侯德榜利用食盐为原料制得了纯碱 |
10.紫甘蓝汁液在不同酸碱度下能显示相应的颜色,记录如下
下列物质中,能使紫甘监汁液变黄的是( )

下列物质中,能使紫甘监汁液变黄的是( )
| A. | 氧氧化钠溶液 | B. | 食盐溶液 | C. | 硫酸溶液 | D. | 水 |
17.某久置的NaOH固体中水的质量分数为3.4%,Na2CO3质量分数为10.6%,其它均为NaOH.向20克的此样品中加入过量的稀盐酸,完全反应后再加入12克10%的NaOH溶液,恰好完全中和,则所得溶液中溶质质量为( )
| A. | 26.91 g | B. | 2.34g | C. | 29.25g | D. | 32.05g |