题目内容
17.某久置的NaOH固体中水的质量分数为3.4%,Na2CO3质量分数为10.6%,其它均为NaOH.向20克的此样品中加入过量的稀盐酸,完全反应后再加入12克10%的NaOH溶液,恰好完全中和,则所得溶液中溶质质量为( )| A. | 26.91 g | B. | 2.34g | C. | 29.25g | D. | 32.05g |
分析 稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,和氢氧化钠反应生成氯化钠和水;
所得溶液中溶质是氯化钠,根据提供的数据可以计算钠元素的质量,进一步可以计算溶质氯化钠的质量.
解答 解:设溶液中氯化钠的质量为x,
20g此样品中钠元素的质量为:20g×10.6%×$\frac{46}{106}$×100%+20g×(1-3.4%-10.6%)×$\frac{23}{40}$×100%+12g×10%×$\frac{23}{40}$×100%=11.5g,
x×$\frac{23}{58.5}$×100%=11.5g,
x=29.25g,
故选:C.
点评 解答的关键是反应前后钠元素的质量不变,完全转化到氯化钠中,要注意理解.

练习册系列答案
相关题目
8.一包固体可能含有硫酸钠、氯化铜、碳酸钙和氯化钠中的一种或几种.根据以下实验得出的结论错误的是( )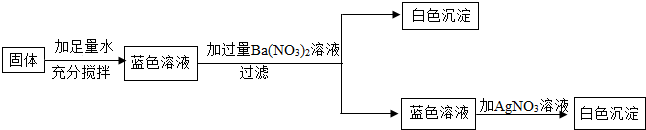

| A. | 一定有硫酸钠 | B. | 一定没有碳酸钙 | ||
| C. | 可能有氯化钠 | D. | 一定有氯化铜和氯化钠 |
12.实验室用加热氯酸钾的方法制取氧气并用排水法收集,下列仪器在组装时的前后顺序正确的是( )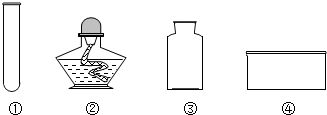

| A. | ②①④③ | B. | ①②④③ | C. | ①②③④ | D. | ②①③④ |
9.O2-被称为“空气维生素”.有关O2-说法正确的是( )
| A. | 属于阳离子 | B. | 属于氧分子 | ||
| C. | 相对分子质量为32g | D. | 属于阴离子 |
7.我们每天都和化学变化打交道,下列叙述不是化学变化的是( )
| A. | 人吃进的食物逐渐被消化 | B. | 蔬菜腐烂 | ||
| C. | 使用煤气作燃料烧饭做菜 | D. | 水在冰箱里结成冰 |
 如图是同学们在实验室制取气体,并进行气体的性质检测用到的仪器,请回答相关问题.
如图是同学们在实验室制取气体,并进行气体的性质检测用到的仪器,请回答相关问题.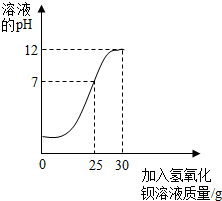 为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算:
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算: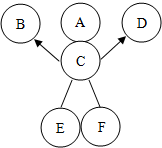 如图中的六个原A、B、C、D、E、F分别表示六种物质,蓝色溶液A与C反应能生成两种沉淀,B为氧化物,D、E、F分别是碳酸钠溶液、稀硫酸和氢氧化钠溶液中的一种,E中溶质可用于生产洗涤剂,用“→”表示一种物质能转化为另一种物质,用两个圆相切或“--”表示两种物质可以发生化学反应,六种物质之间的部分反应及转化关系如图所示.请利用初中化学知识回答下列问题:
如图中的六个原A、B、C、D、E、F分别表示六种物质,蓝色溶液A与C反应能生成两种沉淀,B为氧化物,D、E、F分别是碳酸钠溶液、稀硫酸和氢氧化钠溶液中的一种,E中溶质可用于生产洗涤剂,用“→”表示一种物质能转化为另一种物质,用两个圆相切或“--”表示两种物质可以发生化学反应,六种物质之间的部分反应及转化关系如图所示.请利用初中化学知识回答下列问题: 某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为63.4g.
某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为63.4g.